
向一定物质的量的Fe3O4和Fe的混合物中加50mL 2mol·L-1H2SO4,恰好使之完全溶解,并放出448mL(标况)气体。在所得溶液中加入KSCN溶液,不变红色,则用足量的CO在高温下与相同质量的此混合物反应,能得到多少克铁?
5.6g
按常规思路,应先求出Fe3O4和Fe的物质的量。
设此混合物中Fe3O4和Fe的物质的量分别为x和y,有
![]()
Fe + H2SO4====FeSO4+H2↑
0.02mol 0.02mol 0.02mol
Fe3O4+4H2SO4====FeSO4+Fe2(SO4)3+4H2O
x 4x x
所得溶液加入KSCN溶液不变红色,表明必然发生如下反应
Fe+Fe2(SO4)3====3FeSO4
x x
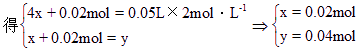
Fe3O4+4CO![]() 3Fe+4CO2
3Fe+4CO2
0.02mol 0.06mol
故能得到铁的质量为(0.04+0.06)mol×56g·mol-1=5.6g
解答本题还可用电荷守恒原则和质量守恒定律,使运算过程化简。据Fe3O4和Fe溶于H2SO4后全部转化为FeSO4,则n(Fe2+)=n(SO42-)=n(Fe)=2mol·L-1×0.05L=0.1mol m(Fe)=0.1mol×56g·mol-1=5.6g。


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源:物理教研室 题型:038
向一定物质的量的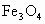 和Fe的混合物中加入
和Fe的混合物中加入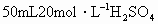 溶液,在一定条件下恰好使混合物完成溶解,放出448mL(标准状况)的气体.在所得溶液中加入KSCN溶液,无红色出现,那么用足量的CO在高温下与相同质量的此混合物充分反应,能得到铁的质量是多少?
溶液,在一定条件下恰好使混合物完成溶解,放出448mL(标准状况)的气体.在所得溶液中加入KSCN溶液,无红色出现,那么用足量的CO在高温下与相同质量的此混合物充分反应,能得到铁的质量是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定物质的量的Fe3O4和Fe的混合物中加入50 mL 2 mol·L-1 H2SO4溶液,在一定条件下恰好使混合物完全溶解,放出448 mL(标准状况)的气体。在所得溶液中加入KSCN溶液,无红色出现,那么,用足量的CO在高温下与相同质量的此混合物充分反应,能得到铁的质量为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com