
判断正误,正确的划“√”,错误的划“×”
(1)铝在自然界中有游离态和化合态两种形式 ( )
(2)Mg、Al在空气中性质稳定,因而都具有很强的抗腐蚀性 ( )
(3)MgO与Al粉的混合物也可称为铝热剂 ( )
(4)Mg是活泼金属,而Al是两性金属 ( )
科目:高中化学 来源: 题型:
化学是一门实用性强的自然科学,在社会、生产、生活中起着重要的作用,下列说法正确的是
A.金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti
B. 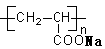 表示一种吸水性高分子树脂
表示一种吸水性高分子树脂
C.用于现代建筑的钢筋混凝土不属于复合材料
D.山东东营广饶县一男子收到网购物品后,因吸入氟乙酸甲酯中毒身亡,氟乙酸甲酯的结构
简式为FCH2COOCH3,能与H2发生加成反应,也能被LiAlH4还原
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于可逆反应的叙述正确的是:
A.可逆反应是指既能向正反应方向进行,同时又能向逆反应方向进行的反应
B.2H2O 2H2+O2与2H2+O2
2H2+O2与2H2+O2 2H2O互为可逆反应
2H2O互为可逆反应
C.对于可逆反应,当正反应速率增大时,逆反应速率就会减小
D.外界条件对可逆反应的正、逆反应速率影响的程度不一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
有Fe2+、NO3-、Fe3+、NH4+、H+、H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
A.氧化剂中心原子的杂化方式为sp2
B.还原剂的外围电子排布式为3d54s1
C.还原产物的VSEPR模型为正四面体
D.该反应可设计为原电池,其负极反应为Fe2+- e-= Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为周期表的一部分,其中的编号代表对应的元素。试填空。

(1)元素A分别与E、F、G形成最简单的常见化合物分子甲、乙和丙。下列有关叙述不正确的有________。
A.甲、乙和丙分子均为由极性键构成的极性分子
B.甲、乙和丙分子中,中心原子均采取sp3的杂化方式
C.三种分子中键角由大到小的顺序是甲>乙>丙
D.甲、乙和丙分子的空间构型分别为正四面体形、三角锥形、V形
(2)元素B基态原子中电子共占据了 个轨道,其价电子排布式为 。
(3)工业上制取D的单质时,并不采取电解D与I的化合物的方法,原因是 。
(4)在测定A与H形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是________________________________________________。
(5)化合物CI3的溶液贮存较长时间,往往出现浑浊,原因是 (用离子方程式表示)。
(6)化合物(EF)2的性质与卤素单质相似,根据共价键理论推测,该分子中σ键和π键数目之比为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
合金是建造航空母舰的主体材料。
航母升降机可由铝合金制造。
①铝元素在周期表中的位置_______________________________________________,
工业炼铝的原料由铝土矿提取而得,提取过程中通入的气体为______________。
②AlMg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为____________________。焊接过程中使用的保护气为__________________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。请回答下列问题:
(1)水分子中氧原子在基态时核外电子排布图为 ;
(2)把HCl气体、NaCl固体、蔗糖分别溶于水,其中化学键发生变化的是 ;
(3)常温下把HCl气体溶于水制得0.1mol/L盐酸,该溶液中由水电离出的氢离子浓度为
mol/L;
(4)常温下把FeCl3固体溶于水,溶液的pH 7(填“大于”“小于”或“等于”),用离子方程式解释原因: ;把该溶液蒸干并灼烧,所得物质的化学式为 ;
(5)水既有氧化性又有还原性,请写出一个表现水的氧化性的化学方程式:
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,此配合离子的化学式是 ;向该蓝色溶液中加入少量氨水,现象为 ,继续加入过量氨水会产生 现象,原因
是 (用化学方程式或离子方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com