
 某科研机构用NaOH溶液吸收硫酸工业废气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到某种副产物,其原理如图所示(电极材料为石墨).
某科研机构用NaOH溶液吸收硫酸工业废气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到某种副产物,其原理如图所示(电极材料为石墨).分析 (1)当有1 mol Na+通过阳离子交换膜时,说明整个电路中转移1mol的电子,而a极是阴极,电极式为:2 H++2e-=H2↑,所以生成气体的物质的量为0.5mol,所以体积为为0.5mol×22.4L/mol=11.2L,L(标准状况),阳极是亚硫酸根离子发生氧化反应,其电极反应式是 SO32--2e-+H2O═SO42-+2H+;
(2)稀NaOH溶液的作用是增强溶液的导电性,B处流出较浓的NaOH溶液,C处是b极阳极是亚硫酸根离子发生氧化反应,其电极反应式是 SO32--2e-+H2O═SO42-+2H+,则流出的是较浓的硫酸;
(3)根据得失电子,C H4~4 SO2进行计算求解.
解答 解:(1)当有1 mol Na+通过阳离子交换膜时,说明整个电路中转移1mol的电子,而a极是阴极,电极式为:2 H++2e-=H2↑,所以生成气体的物质的量为0.5mol,所以体积为为0.5mol×22.4L/mol=11.2L,L(标准状况),阳极是亚硫酸根离子发生氧化反应,其电极反应式是 SO32--2e-+H2O═SO42-+2H+,故答案为:11.2;SO32--2e-+H2O═SO42-+2H+;
(2)稀NaOH溶液的作用是增强溶液的导电性,B处流出较浓的NaOH溶液,C处是b极阳极是亚硫酸根离子发生氧化反应,其电极反应式是 SO32--2e-+H2O═SO42-+2H+,则流出的是较浓的硫酸,故答案为:增强溶液导电性;较浓的硫酸;
(3)C H4~4 SO2
1 4
V 40×20%
所以V=2,故答案为:2.
点评 本题考查了电解原理、电极方程式的书写等知识,注意知识的归纳和梳理是关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 77 | B. | 37 | C. | 191 | D. | 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K3C60中只有离子键 | B. | K3C60中不含共价键 | ||
| C. | 该晶体在熔融状态下能导电 | D. | C60与12C互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
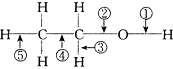
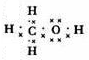 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
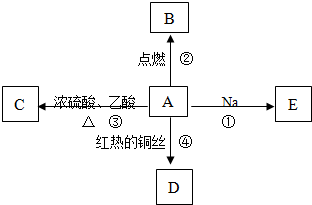
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ClO3->BrO3->Cl2>Fe3+>I2 | B. | BrO3->Cl2>ClO3->I2>Fe3+ | ||
| C. | BrO3->ClO3->Cl2>Fe3+>I2 | D. | BrO3->ClO3->Fe3+>Cl2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH3(CH2)4CH3 | B. | CH3CH2CHO | C. | CH3CH=CHCH3 | D. | (CH3)3C-C≡C-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①② | C. | ①③ | D. | ②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com