
【题目】已知元素X的基态原子最外层电子排布式为nsn-1npn+2,则X元素的原子序数为
A. 9 B. 10 C. 17 D. 18
科目:高中化学 来源: 题型:
【题目】将1 mol I2(g) 和2 mol H2置于2L密闭容器中,在一定温度下发生反应:I2(g) + H2(g) ![]() 2HI(g) △H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:
2HI(g) △H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:

(1)达平衡时,I2(g)的物质的量浓度为mol/L 。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示。则甲条件可能是 ,则乙条件可能是 。(填入下列条件的序号)
①恒容条件下,升高温度;②恒容条件下,降低温度;③恒温条件下,缩小反应容器体积;④恒温条件下,扩大反应容器体积;⑤恒温恒容条件下,加入正催化剂。
(3)若保持温度不变,在另一个相同的2L密闭容器中加入2mol I2(g)、4mol H2(g)发生反应,达平衡时,HI的体积分数是 0.6(填大于、等于、小于)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A.1 L 1 mol L—1硫酸溶液中所含的氧原子数为4NA
B.标准状况下,11.2 L CC14中所含的原子数为2.5NA
C.2.7 g A1与足量氧气充分反应,转移的电子数为0.3NA
D.常温常压下,14 g由N2与CO组成的混合气体中所含的原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是 。
(2)该反应中,发生还原反应的过程是 (填氧化剂)→ 。(填还原产物)
(3)写出该反应的化学方程式,并用单线桥法标出电子转移的方向和数目:
(4)如反应转移0.3mol电子,则产生的气体在标准状况下体积为 L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原子核外电子排布式或运动状态的描述中,不完全是专指碳原子的是( )
A. 原子核外电子有六种运动状态
B. L能层p能级只有一个空轨道
C. L能层有两个未成对的电子
D. 最外层p能级电子数与次外层电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某10% NaOH溶液,加热蒸发掉100g水后得到80mL 20%的溶液,则该20% NaOH溶液的物质的量浓度为( )
A.7 mol/L B.12.5 mol/L C.6.25 mol/L D.7.5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
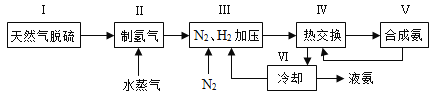
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:____________________。
(2)步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g)![]() CO(g)+3H2(g)ΔH=+206.4kJ·mol-1
CO(g)+3H2(g)ΔH=+206.4kJ·mol-1
②CO(g)+H2O(g)![]() CO2(g)+H2(g)ΔH=-41.2kJ·mol-1
CO2(g)+H2(g)ΔH=-41.2kJ·mol-1
对于反应①,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是 __。
利用反应②,将CO进一步转化,可提高H2的产量。若1 mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18 mol CO、CO2和H2的混合气体,则CO的转化率为____________。
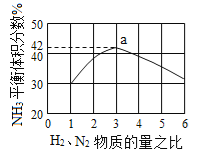
(3)图(a)表示500 ℃、60.0 MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:____________。
(4)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)_____________。简述本流程中提高合成氨原料总转化率的方法:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.含有离子键的化合物必是离子化合物
B.含有共价键的化合物就是共价化合物
C.共价化合物可能含离子键
D.离子化合物中一定含有共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com