
 短周期主族元素X、Y、Z、W 的原子序数依次增大,X、Y、Z原子序数之和是W的2倍,X、Z在周期表中的相对位置如图所示,X的最低负价绝对值与其原子最外层电子数相等.下列说法正确的是( )
短周期主族元素X、Y、Z、W 的原子序数依次增大,X、Y、Z原子序数之和是W的2倍,X、Z在周期表中的相对位置如图所示,X的最低负价绝对值与其原子最外层电子数相等.下列说法正确的是( )| A、原子半径:r(Y)>r(Z)>r(W) |
| B、Y、Z、W的简单离子的电子层结构相同 |
| C、XWm与YWn中化学键类型相同(m、n为正整数) |
| D、元素Z的简单气态氢化物的热稳定性比W的简单气态氢化物强 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
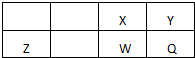 短周期元素X、Z、W、Q在元素周期表中的位置如图所示,其中X、Z元素最外层电子数是最内层电子数的2倍,则下列说法正确的是( )
短周期元素X、Z、W、Q在元素周期表中的位置如图所示,其中X、Z元素最外层电子数是最内层电子数的2倍,则下列说法正确的是( )| A、X、W能与钠形成摩尔质量相同的化合物,且阴阳离子数比为2:1 |
| B、含X和Z元素的常见化合物为分子晶体 |
| C、Y单质能从Q的钠盐溶液中置换出Q单质 |
| D、半径大小关系:W离子>Q离子>W原子>Q原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
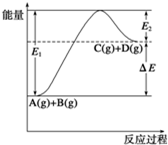
| A、1mol A与1mol B充分反应后,能量变化为△E |
| B、加入催化剂后,反应加快,△E减小 |
| C、反应物的总键能小于生成物的总键能 |
| D、反应达到平衡时,升高温度,A的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 的叙述正确的是( )
的叙述正确的是( )| A、均能用CnH2n+2组成通式来表示 |
| B、与所有烷烃互为同素异形体 |
| C、因为它们结构相似,所以它们的化学性质相似,物理性质相同 |
| D、通常情况下它们都是气态烷烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不能用植物油萃取溴水中的溴 |
| B、皂化是高分子生成小分子的过程 |
| C、和H2加成后能提高其熔点及稳定性 |
| D、水解可得到丙三醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HF的沸点比HCl的沸点高,是由于HF分子间存在氢键作用 |
| B、H2O加热到很高温度都难以分解,是因为水分子间有氢键作用 |
| C、水在结冰时体积膨胀,是由于水分子间存在氢键作用 |
| D、在氨水中水分子和氨分子之间也存在着氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2011年3月11日,日本发生大地震,并引发核电厂爆炸,核反应属于物理变化 |
| B、“光化学烟雾”、“臭氧空洞”、“硝酸酸雨”的形成都与氮氧化合物有关 |
| C、低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放 |
| D、高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com