
| A、133Cs的核电荷数为133 |
| B、铯与水的反应比钠与水的反应缓慢 |
| C、133Cs原子核外有78个电子 |
| D、133Cs和137Cs互为同位素 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
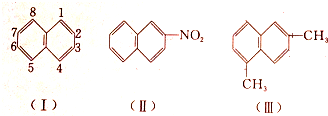
| A、2,6-二甲基萘 |
| B、1,4-二甲基萘 |
| C、4,7-二甲基萘 |
| D、1,6-二甲基萘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③②⑤④ |
| B、②③①④⑤ |
| C、⑤④①③② |
| D、⑤①④③② |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2能与H2S反应生成S |
| B、HCl在水中的溶解度大于H2S |
| C、HCl的酸性强于H2S |
| D、HCl的还原性强于H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol 甲基所含电子数为10NA |
| B、0.1mol的白磷(P4)或甲烷中所含的共价键数均为0.4NA |
| C、在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数均为NA |
| D、标准状况下,2.24L 辛烷完全燃烧,生成CO2分子数为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、本饮料不含任何化学物质 |
| B、饮用水越纯越好,本蒸馏水绝对纯净,不含任何离子 |
| C、本口服液含丰富的氮、磷、锌等微量元素 |
| D、没有水就没有生命 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第ⅠA族元素的金属性比第ⅡA族元素的金属性强 |
| B、同周期非金属氧化物对应水化物的酸性从左到右依次增强 |
| C、第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
| D、第三周期元素的离子半径从左到右逐渐减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com