


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
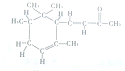
| A、α-鸢尾酮可与某种酚互为同分异构体 |
| B、1mol α-鸢尾酮最多可与2mol H2加成 |
| C、α-鸢尾酮能发生银镜反应 |
D、α-鸢尾酮经加氢→消去反应可转变为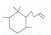 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
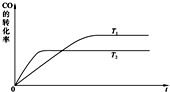 煤间接液化是煤化工的一种重要方法:首先将原料煤与氧气、水蒸汽反应将煤全部气化,制得的粗煤气经变换、脱硫、脱碳制成洁净的合成气(CO+H2),然后合成气在催化剂作用下发生合成反应生成烃类,如:[nCO+(2n+1)H2=CnH2n+2+nH2O];或者合成醇类,如合成甲醇:CO(g)+2H2(g)?CH3OH(g).等等.
煤间接液化是煤化工的一种重要方法:首先将原料煤与氧气、水蒸汽反应将煤全部气化,制得的粗煤气经变换、脱硫、脱碳制成洁净的合成气(CO+H2),然后合成气在催化剂作用下发生合成反应生成烃类,如:[nCO+(2n+1)H2=CnH2n+2+nH2O];或者合成醇类,如合成甲醇:CO(g)+2H2(g)?CH3OH(g).等等.| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、冬天在汽车水箱中加乙二醇抗冻 |
| B、蚂蚁叮咬的红肿处涂沫苯酚止痒 |
| C、纺织品上的油渍用烧碱溶液清洗 |
| D、把铁器具浸入水中隔绝空气防生锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C是中学化学中常见的单质,常温下甲、乙两种化合物分别是黑色固体和无色液体,这些化合物和单质之间有如图所示关系.据此判断:
A、B、C是中学化学中常见的单质,常温下甲、乙两种化合物分别是黑色固体和无色液体,这些化合物和单质之间有如图所示关系.据此判断:查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E五种元素均为短周期元素,原子序数逐渐增大,A元素原子的核外电子数、电子层数和最外层电子数均相等.B、C、D、E三种元素在周期表中相对位置如表,只有E元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的若干种组成(只有M分子同时含有三种元素),其中甲、乙为非金属单质,W由A和C组成,分子中含有18个电子,X分子含有10个电子,它们之间的相互转化关系如图:
A、B、C、D、E五种元素均为短周期元素,原子序数逐渐增大,A元素原子的核外电子数、电子层数和最外层电子数均相等.B、C、D、E三种元素在周期表中相对位置如表,只有E元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的若干种组成(只有M分子同时含有三种元素),其中甲、乙为非金属单质,W由A和C组成,分子中含有18个电子,X分子含有10个电子,它们之间的相互转化关系如图:| B | C | D | |
| E |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com