
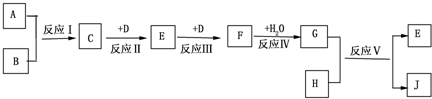
分析 A、B、D、H是中学化学中常见的单质,J为蓝色溶液,应含有铜离子,根据各物质的转化关系,
(1)若A、B均为气体时,当用玻璃棒分别蘸取C、G的浓溶液并使它们靠近时,有白烟生成,应为HCl或HNO3和NH3的反应生成NH4Cl,由于C连续与单质D反应后又与水反应生成G,则C为NH3,D为O2,E为NO,F为NO2,G为HNO3,A、B应为氮气和氢气,硝酸与铜反应生成硝酸铜和NO,所以H为Cu,J为Cu(NO3)2;(2)若A为气体,B为固体时,已知C在D中完全燃烧可生成E和水,E是一种常见的空气污染物,且将C与E混合可生成淡黄色固体B,则A为H2,B为S,C为H2S,D为O2,E为SO2,F为SO3,G为H2SO4,硫与铜反应生成硫酸铜和SO2,所以H为Cu,J为CuSO4,据此答题.
解答 解:A、B、D、H是中学化学中常见的单质,J为蓝色溶液,应含有铜离子,根据各物质的转化关系,
(1)若A、B均为气体时,当用玻璃棒分别蘸取C、G的浓溶液并使它们靠近时,有白烟生成,应为HCl或HNO3和NH3的反应生成NH4Cl,由于C连续与单质D反应后又与水反应生成G,则C为NH3,D为O2,E为NO,F为NO2,G为HNO3,A、B应为氮气和氢气,硝酸与铜反应生成硝酸铜和NO,所以H为Cu,J为Cu(NO3)2,
①根据上面的分析可知,D为O2,E为NO,
故答案为:O2;NO;
②反应Ⅱ的化学方程式为4NH3+5O2$\frac{\underline{\;催化剂\;}}{高温}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{\;催化剂\;}}{高温}$4NO+6H2O;
(2)若A为气体,B为固体时,已知C在D中完全燃烧可生成E和水,E是一种常见的空气污染物,且将C与E混合可生成淡黄色固体B,则A为H2,B为S,C为H2S,D为O2,E为SO2,F为SO3,G为H2SO4,硫与铜反应生成硫酸铜和SO2,所以H为Cu,J为CuSO4,C与E反应的化学方程式为2H2S+SO2=3S+2H2O,检验气体SO2的方法是将气体体SO2通入品红溶液,溶液褪色,加热后恢复红色,证明E是SO2,
故答案为:2H2S+SO2=3S+2H2O;将气体体SO2通入品红溶液,溶液褪色,加热后恢复红色,证明E是SO2.
点评 本题考查无机物的推断,题目难度中等,物质的颜色以及反应现象为推断突破口,需要学生熟练掌握元素化合物性质.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:多选题
| A. | 铜的金属活泼性比铁的弱,可在海轮外壳上镶入若干铜块以减缓海轮腐蚀 | |
| B. | 为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 | |
| C. | 实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 | |
| D. | 吸热反应TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)在一定条件下可自发进行,则该反应的△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg失火不能用CO2灭火;Na失火也不能用CO2灭火 | |
| B. | Fe3O4可写成FeO•Fe2O3;Pb3O4也可以写成PbO•Pb2O3 | |
| C. | 不能用电解熔融AlCl3来制取金属铝;但能用电解熔融MgCl2来制取金属镁 | |
| D. | Fe与S直接化合生成FeS;Al与S也可以直接化合得到Al2S3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠的多 | B. | 铁的多 | ||
| C. | 铁和钠放出一样多 | D. | 无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2012年世界青年奥运会将在南京举办.保护环境,人人有责.
2012年世界青年奥运会将在南京举办.保护环境,人人有责.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 测得某工业废水中含有乙酸钠及对氯酚(
测得某工业废水中含有乙酸钠及对氯酚(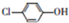 ),为改善水质现利用微生物电池加以去除,反应原理如图所示,下列说法正确的是( )
),为改善水质现利用微生物电池加以去除,反应原理如图所示,下列说法正确的是( )| A. | X极为微生物电池的负极 | |
| B. | 该电池能够在高温下工作 | |
| C. | 图中离子交换膜应为阴离子交换膜 | |
| D. | Y极电极反应式为:CH3COO--8e-+4H2O═2HCO3-+9H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com