
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2014届河北省高三调研考试理综化学试卷(解析版) 题型:填空题
标准状况下,1体积水中能溶解500体积的HCl气体。若向1 L水中通入标准状况下的448 L HCl气体,假设气体完全溶解。
(1)若所得溶液密度为1.2 g/cm3,则溶液中含HCl物质的量浓度为 ;
(2)从该溶液中取出10 mL浓盐酸溶解于水配制成500 mL溶液,配制后的稀溶液中含HCl物质的量浓度为 。
(3)在用浓盐酸配制上述稀盐酸时,所用仪器中,使用前必须检查是否漏液的仪器有 ;配制过程中,造成浓度偏低的操作可能有_______________(选填下列操作的序号)。
A、容量瓶蒸馏水洗后未加干燥
B、量筒用蒸馏水洗后未干燥
C、将烧杯中浓盐酸移入容量瓶后,未用水洗涤烧杯,即向容量中加水到刻度
D、用胶头滴管向容量瓶中加水时,不慎超过刻度线,用另外胶头滴管从瓶中吸出部分溶液使剩余溶液刚巧达刻度线
E、定容时,俯视液面加水至刻度线
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖南省长沙市高三第六次月考化学试卷 题型:实验题
可溶性氯化物中氯含量的测定常采用莫尔法,此法是以K2CrO4为指示剂,用AgNO3标准溶液进行滴定。其实验步骤为:
一、配制0.100mol·L-1AgNO3溶液
准确称取AgNO38.50g,溶于500mL不含氯离子的蒸馏水中,摇匀后,贮存于带玻璃塞的棕色试剂瓶中。
二、0.100mol·L-1AgNO3溶液的标定
准确称取0.585g NaCl于100mL烧杯中,用蒸馏水溶解后,定量转移入100mL容量瓶中,加水稀释至刻度,摇匀。
取所配NaCl溶液25.00mL 3份,分别置于锥形瓶中,加25mL水,1mL 5% K2CrO4溶液,在不断摇动下用AgNO3溶液滴定,至溶液呈砖红色[2Ag++CrO===Ag2CrO4↓(砖红色)]。实验测得三次所耗硝酸银溶液体积的平均值为26.32mL。
三、氯化物试样中氯的测定
准确移取25.00mL氯化物试液3份,分别置于锥形瓶中,加入25mL水,1mL 5% K2CrO4溶液,在不断摇动下用AgNO3标准溶液滴定至溶液呈砖红色。实验测得三次所耗硝酸银溶液的体积的平均值为VmL。
回答下列问题:
(1)NaCl固体使用前,要将其置于坩埚中加热,并用 不断搅拌,以除掉氯化钠晶体中的水。
(2)AgNO3溶液需要标定的主要原因是 。
(3)指示剂CrO在溶液中存在下列的平衡:2H++2CrO 2HCrO
2HCrO Cr2O+H2O,由此判断该滴定适宜的pH值范围可能是 。(填代号)
Cr2O+H2O,由此判断该滴定适宜的pH值范围可能是 。(填代号)
A.1——6.5 B.6.5——10.5 C.10.5——14
(4)用硝酸银滴定氯离子达到化学计量点时,c(Ag+)=c(Cl-),若此时要求不生成Ag2CrO4沉淀,c(CrO)最大不能超过 mol·L-1,因此,实验中对指示剂的浓度有较高的要求。(已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.8×10-12)
(5)CrO的黄色对滴定终点的判断没有影响的原因是 。
(6)AgNO3标准溶液的准确浓度为 mol·L-1,列出计算可溶性氯化物试液中氯元素的含量的式子: g·L-1。
查看答案和解析>>
科目:高中化学 来源:2012届浙江省高二下二学期期中考试化学试卷 题型:填空题
(10分)已知几种难溶电解质的溶度积如下表所示:
|
几种难溶电解质的Ksp(25℃) |
|
|
沉淀溶解平衡 |
Ksp |
|
AgBr(s) |
5,0×10-13mol2·L-2 |
|
AgI(s) |
8.3×10-17mol2·L-2 |
|
FeS(s) |
6.3×10-18mol2·L-2 |
|
ZnS(s) |
1.6×10-24mol2·L-2 |
|
CuS(s) |
1.3×10-36mol2·L-2 |
(1)AgBr、AgI、FeS、ZnS、CuS的溶解能力由大到小的顺为: 。
(2)向饱和的AgI溶液中加入固体硝酸银,则c(I-) (填“增大”、“减小”或“不变”),若改加AgBr固体,则c(Ag+) (填“增大”、“减小”或“不变”)。
(3)在25℃时,向100mL浓度均为0.1 mol·L-1 FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是 (用沉淀物的化学式表示)。
(4)在25℃时,把ZnS加入蒸馏水中,一定时间后达到如下平衡: ZnS(s) Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是 。
Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是 。
A.加入少量CuS固体 B.加入少量FeS固体
C.加入少量FeCl2固体 D.加入少量CuCl2固体
查看答案和解析>>
科目:高中化学 来源:2012届安徽省高二下学期期末联考化学试卷 题型:实验题
(10分)下表是某超市出售的加碘食盐的有关说明:
|
配 料 表 |
精制盐、碘酸钾 |
|
含 碘 量 |
45±5mg/kg |
|
储 藏 方 法 |
通风、防潮 |
|
食 用 方 法 |
根据烹调所需适量加入 |
某研究性学习小组欲通过实验检验该碘盐中是否含碘:
(1)首先取该食盐样品配制室温下的饱和溶液:向200 mL蒸馏水中加入75.0g 该食盐样品,加热并搅拌,直到完全溶解。冷却至室温。(已知室温条件下氯化钠溶解度为36 g)
在加热过程中需要用到的仪器有铁架台、酒精灯、铁圈、____________、烧杯和玻璃棒。冷却至室温过程中若出现____________________(填现象),则证明其为饱和溶液。
(2)甲同学先向该饱和食盐溶液中加入1mol/L的KI溶液和几滴淀粉溶液,然后加入0.1mol/L稀硫酸,振荡,溶液变为蓝色。该实验发生的化学反应中氧化剂与还原剂的物质的量之比为_______________。请在下图中画出参加反应的IO3—的物质的量和析出的I2单质的物质的量的关系曲线。
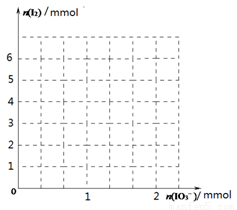
(3)乙同学认为甲同学的实验方案不严谨,他提出如下假设:空气中的氧气可能参与反应,使溶液变蓝。反应的离子方程式为:_____________________________________。
请你设计实验方案验证乙同学的假设是否正确:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com