
 后静置,放出水层(废液).
后静置,放出水层(废液).分析 (1)浓硫酸起到了催化作用和吸水作用;
(2)乙醇和乙酸在浓硫酸加热作用下反应生成乙酸乙酯和水;
(3)饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;乙酸乙酯在强碱性条件下发生水解反应;
(4)饱和CaCl2溶液可以吸收乙酸乙酯中可能残留的乙醇;
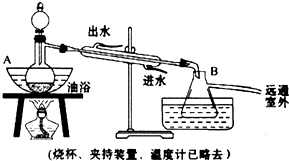
(5)保持蒸馏烧瓶中压强一定,得到平稳的蒸气气流;
(6)酯比水轻,分层后在水溶液上层.
解答 解:(1)乙酸与乙醇发生酯化反应,需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,浓硫酸的作用为催化剂,吸水剂,
故答案为:催化剂、吸水剂;
(2))酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应,反应的化学方程式为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
故答案为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
(3)制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯;洗涤粗酯的饱和Na2CO3溶液改为NaOH溶液,乙酸乙酯在强碱性条件下发生水解反应,致使乙酸乙酯水解,使实验失败,
故答案为:致使乙酸乙酯水解,使实验失败;
(4)饱和CaCl2溶液可以吸收乙酸乙酯中可能残留的乙醇,这样分离出的粗酯中只含有水了,
故答案为:除去乙酸乙酯中的乙醇;
(5)酯比水轻,分层后位于水溶液上层,静置分液,上层液体从分液漏斗上口倒出,
故答案为:上口倒出.
点评 本题考查乙酸乙酯的制备,题目难度中等,涉及的题量较大,注意浓硫酸的作用、饱和碳酸钠溶液、氯化钙溶液的作用以及酯化反应的机理,试题培养了学生分析、理解能力及灵活应用所学知识解决实际问题的能力.


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:选择题
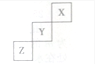
| A. | Z的最高价氧化物的水化物是强酸 | |
| B. | Y是气态氢化物稳定性小于Z的气态氢化物 | |
| C. | Z一定是活泼的金属 | |
| D. | 1molZ单质在足量的氧气中燃烧时,有6mol电子发生转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤⑥ | B. | ②③④⑤ | C. | ①③④⑥ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热 | |
| B. | 加入少量CuSO4溶液 | |
| C. | 不用稀硫酸,改用质量分数为98%的浓硫酸 | |
| D. | 不用铁片,改用铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用足量Br2的四氯化碳溶液除去甲烷中的乙烯 | |
| B. | 蛋白质溶液中加入CuSO4溶液后,蛋白质析出,再加水不溶解 | |
| C. | 苯的硝化反应属于取代反应 | |
| D. | 往溴水中加入苯,振荡,溴水变为无色,说明苯与溴发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 加入试剂 | 实验现象 |
| Ⅰ | 4mL 2mol/L NH4Cl 溶液 | 沉淀溶解 |
| Ⅱ | 4mL蒸馏水 | 沉淀不溶解 |
| 序号 | 实验内容 | 结 果 |
| 1 | 测定醋酸铵溶液的pH | pH约为7,溶液呈中性 |
| 2 | 取少量的相同质量的氢氧化镁分别盛放在试管中,分别向其中滴加醋酸铵溶液和氯化铵溶液 | 固体均溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a:(b+c+d)=1:1.5 | B. | (a+b):(c+d)=1:1 | C. | a=b=c=d=1.12L | D. | a+b+c=d=0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com