
【题目】某温度时,在3L密闭容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据
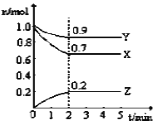
(1)该反应的化学方程式为:______
(2)反应开始至2min,用X表示的平均反应速率为:______;平衡时,Y的转化率为______;平衡时,Y的浓度为______;
(3)在密闭容器里,通入a mol X(s)和b mol Y(g),发生反应X(s)+Y (g)2Z(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)
①增加X(s)的质量:______
②增大容器的体积:______。
【答案】3X+Y![]() 2Z 0.05 mol/(L·min) 10% 0.3mol/L 不变 减小
2Z 0.05 mol/(L·min) 10% 0.3mol/L 不变 减小
【解析】
(1)根据参加反应的物质的物质的量之比等于化学计量数之比书写化学方程式;
(2)根据![]() 及转化率=
及转化率=![]() ×100%计算;
×100%计算;
(3)依据外因对化学反应速率的影响作答。
(1)由图象可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质的量增多,应为生成物,当反应进行到2min时,△n(Y)=1.0 mol -0.9 mol =0.1mol,△n(X)=1.0 mol -0.7 mol =0.3mol,△n(Z)=0.2mol,则△n(X):△n(Y):△n(Z)=3:1:2,因参加反应的物质的物质的量之比等于化学计量数之比,所以反应的方程式为:3X+Y![]() 2Z;
2Z;
(2)反应开始至2min末,X的反应速率为:![]() =0.05 mol/(L·min);平衡时,Y的转化率为
=0.05 mol/(L·min);平衡时,Y的转化率为![]() =10%;平衡时,Y的浓度为
=10%;平衡时,Y的浓度为![]() =0.3 mol/L,故答案为:0.05 mol/(L·min);10%;0.3 mol/L;
=0.3 mol/L,故答案为:0.05 mol/(L·min);10%;0.3 mol/L;
(3)①X为固体,浓度保持不变,则增大X的质量,反应速率不变;
②对于反应X(s)+Y(g)2Z(g)来说增大容器的体积,相当于减小体系压强,则反应速率减小。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列现象不属于蛋白质变性的是
A.打针时用酒精消毒
B.用稀的福尔马林浸泡种子
C.蛋白质溶液中加入食盐变浑浊
D.用波尔多液(主要含有CuSO4)防止作物虫害
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质全部是弱电解质的是( )
A.H2SiO3 H2S CO2B.MgSO4 CH3COOH CH3CH2OH
C.H2SO3 Ca(OH)2 CH3COOHD.H2O NH3H2O H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有以下各组微粒或物质:A.正丁烷和异丁烷;B.金刚石、石墨和C60;C.冰和干冰;D.35Cl和37Cl;E.NO和NO2;其中,互为同分异构体的有__________(填编号,以下同);互为同素异形体的有__________;互为同位素的有__________。
(2)现有:①干冰;②金刚石;③NH4Cl;④Na2S四种物质,按下列要求回答(填序号):熔化时不需要破坏化学键的是____________;既存在离子键又存在共价键的是____________。
(3)向一个容积为2 L的密闭容器中充入7 mol SO2和4 mol O2,在一定温度和压强下,发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g),经4 s后达到平衡状态,测得SO2的物质的量是3 mol,则达到平衡状态时O2的转化率为__________;平衡时SO3的物质的量浓度_______。
2SO3(g),经4 s后达到平衡状态,测得SO2的物质的量是3 mol,则达到平衡状态时O2的转化率为__________;平衡时SO3的物质的量浓度_______。
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个石油化工发展水平的标志。下列是有机物A~G之间的转化关系:

请回答下列问题:
(1)A的官能团的名称是____________。C的结构简式是____________。
(2)E是一种具有香味的液体,由B + D→的反应方程式为:____________。该反应类型是____________。
(3)G是一种高分子化合物,其名称是____________,链节是____________。
(4)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F(沸点12.27OC)进行应急处理。写出由A制F的化学反应方程式:____________。决定F能用于冷冻麻醉应急处理的性质是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组模拟工业制漂白粉,设计了下列图的实验装置。已知:①氯气和碱反应放出热量。②6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O。
5CaCl2+Ca(ClO3)2+6H2O。
回答下列问题:
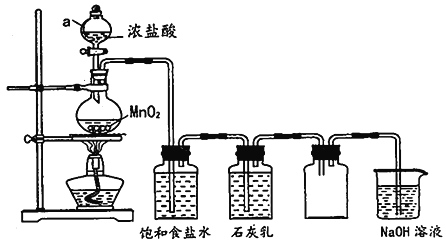
(1)甲装置中仪器a的名称是_____________________。
(2)装置乙中饱和食盐水的作用是_____________________。
(3)①制取漂白粉的化学方程式是______________________________。
②该小组制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],则产物中还混杂有物质的化学式是_____。
③为提高Ca(ClO)2的含量,可采取的措施是__________________(任写一种即可)。
(4)漂白粉应密封保存,原因是______________(用化学方程式表示)。
(5)家庭中常用84 消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)清洁卫生。两者同时混合使用会产生有毒的氯气,写出该反应的离子方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中既能与盐酸反应又能与氢氧化钠溶液反应的是( )
A. Al(OH)3 B. Fe(OH)3 C. Mg(OH)2 D. Cu(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院成功开发出一种新型铝石墨双离子电池,大幅提升了电池的能量密度。该电池放电时的总反应为: AlLi+CxPF6![]() Al+xC+Li++PF6,有关该电池说法正确的是
Al+xC+Li++PF6,有关该电池说法正确的是
A. 充电时,PF6向阳极移动
B. 充电时,铝电极质量减少
C. 放电时,正极反应式为:Al+Li++e![]() AlLi
AlLi
D. 放电时,电子由石墨沿导线流向铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数值。下列说法正确的是
A. 标准状况下,11.2L的甲醇所含的氢原子数等于2NA
B. 25℃时,Ksp(BaSO4)=1×10-10,则BaSO4饱和和溶液中Ba2+数目为1×10-5NA
C. 常温常压下,Na2O2与H2O反应生成1molO2时,转移电子数是2 NA
D. 1L1mol·L-1AlCl3溶液中含有的Al3+数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com