
|


 ������ҵ��ͬ����ϰ��ϵ�д�
������ҵ��ͬ����ϰ��ϵ�д� С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���ݻ��̶����ܱ������У�������Ӧ��CO��g��+2H2��g��?CH3OH��g��������0����2minʱֻ�ı�һ����������Ӧ������±���
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ����׳��Ƥ�顤����ͬ��ϵ�С������ɽ��������߶���ѧ���ϣ� ���ͣ�022
��һ���ݻ��̶��ķ�Ӧ�����У���һ�����һ������ܷ���壬����ֱ���п��淴Ӧ�������ʵ���ʼ���������£�MΪ2.5mol��NΪ3mol��PΪ0mol��A��C��D��Ϊ0.5mol��BΪx mol����x��һ����Χ�ڱ仯ʱ��������ͨ�����ڷ�Ӧ�����¶ȣ�ʹ���෴Ӧ���ﵽƽ�⣮���Ҹ���ǡ�ô��ڷ�Ӧ��������λ�ã���ͼ��ʾ��

���ﵽƽ����Mת����Ϊ75%������д���пհף�
(1)�ﵽƽ���Ӧ�����������ܵ����ʵ���Ϊ________mol��
(2)��ʹ���ҷ�Ӧ��ʼʱ��v(��)��v(��)��x��ȡֵ��Χ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������ش�1��~��3���⡣
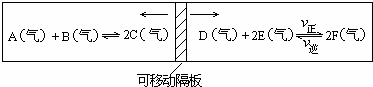
��һ���ݻ��̶��ķ�Ӧ������һ�����һ������ܷ���壬����ֱ������ͼ��ʾ�Ŀ��淴Ӧ��
2A(g)+B(g)=2C(g) | D(g)+3E(g)=2F(g) |
�����ʵ���ʼ���������£�A��B��C��D��E��F�����ʵ����ֱ�Ϊ2mol��1mol��0 mol��Xmol��Ymol��Zmol�����߷�Ӧ��ƽ�����ǡ�������м��λ�á�
��1������ʱ��������������г���0.3mol He(He����A��B��C��D��E��F��Ӧ)������˵����ȷ����
A��A�����ʵ������ӡ� �������������������������� B��B��ת��������
C��C�����ʵ������䡡 �������������������������� D��F��Ũ�ȣ��������һ��������
��2������ʱ���������������ͨ�˵IJ���He������2 molA��1mol B�����壬������˵����ȷ����
�� A��A�������������
�� B��B��ת���ʽ���
�� C��C�����������Ũ�ȶ�����
�� D���ұ�����������ƽ����Է�����������
��3������ʱ�ڣ�2�����ƽ����ϵ�У�����������������ͬʱ�ٸ�ע��lmolHe��ƽ����루2�����ƽ����ϵ��ȣ�����˵����ȷ����
�� A��C��F��Ũ�ȶ�����
�� B��B��ת���ʣ�F�ķֽ��ʶ�������
�� C��A��D���ʵ�����������
�� D��A��B��C��D��E��F���ʵ���������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com