
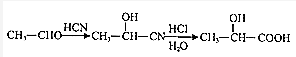
 .
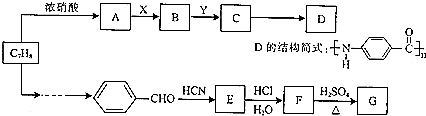
.分析 由D的结构简式可知,C发生缩聚反应生成D,故C为 ,甲苯发生硝化反应生成A,A经过系列反应得到C,可知A为
,甲苯发生硝化反应生成A,A经过系列反应得到C,可知A为 ,由于氨基易被氧化,故应先将甲基氧化为羧基,再将硝基还原为氨基,故X可以是酸性高锰酸钾溶液,Y为Fe/HCl,则B为
,由于氨基易被氧化,故应先将甲基氧化为羧基,再将硝基还原为氨基,故X可以是酸性高锰酸钾溶液,Y为Fe/HCl,则B为 ;
;
甲苯通过一系列反应生成苯甲醛,苯甲醛和HCN发生信息II的反应生成E,E结构简式为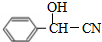 ,E发生水解反应生成F为
,E发生水解反应生成F为 ,F在浓硫酸作用生成含三个六元环的酯类化合物G,应是2分子F发生酯化反应生成环酯,则G为
,F在浓硫酸作用生成含三个六元环的酯类化合物G,应是2分子F发生酯化反应生成环酯,则G为 ,据此分析解答.
,据此分析解答.
解答 解:由D的结构简式可知,C发生缩聚反应生成D,故C为 ,甲苯发生硝化反应生成A,A经过系列反应得到C,可知A为
,甲苯发生硝化反应生成A,A经过系列反应得到C,可知A为 ,由于氨基易被氧化,故应先将甲基氧化为羧基,再将硝基还原为氨基,故X可以是酸性高锰酸钾溶液,Y为Fe/HCl,则B为
,由于氨基易被氧化,故应先将甲基氧化为羧基,再将硝基还原为氨基,故X可以是酸性高锰酸钾溶液,Y为Fe/HCl,则B为 ;
;
甲苯通过一系列反应生成苯甲醛,苯甲醛和HCN发生信息II的反应生成E,E结构简式为 ,E发生水解反应生成F为
,E发生水解反应生成F为 ,F在浓硫酸作用生成含三个六元环的酯类化合物G,应是2分子F发生酯化反应生成环酯,则G为
,F在浓硫酸作用生成含三个六元环的酯类化合物G,应是2分子F发生酯化反应生成环酯,则G为 ,
,
(1)A为 ,A中官能团的名称是硝基,故答案为:硝基;
,A中官能团的名称是硝基,故答案为:硝基;
(2)C发生缩聚反应生成D,所以C→D的反应类型为缩聚反应,故答案为:缩聚反应;
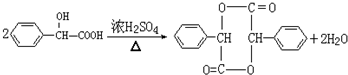
(3)F→G的化学方程式为 ,故答案为:
,故答案为: ;
;
(4)X是酸性高锰酸钾溶液,是为了防止氨基被氧化,故答案为:②;防止氨基被氧化.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析判断及知识迁移、知识综合应用能力,根据生成物、反应物、反应条件及题给信息采用正逆结合的方法进行推断,注意题给信息的正确运用,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 马口铁镀锡的表面即使破损后也能起到很好的防锈作用 | |
| B. | FeCl3饱和溶液滴入到沸水中,并继续煮沸,可得到Fe(OH)3沉淀 | |
| C. | 反应AgCl+NaBr═AgBr+NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水 | |
| D. | 除去某溶液中的SO42-,选择加入可溶性钡盐要比加入钙盐好 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
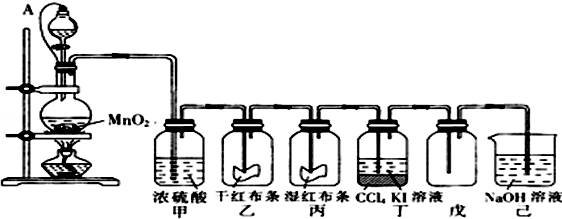
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 比例模型 可以表示CO2分子或SiO2分子 可以表示CO2分子或SiO2分子 | |
| B. | 次氯酸的结构式:H-Cl-O | |
| C. | HCO3-的电离方程式:HCO3-+H2O?CO32-+H3O+ | |
| D. | 含18个中子的氯原子的核素符号:${\;}_{35}^{17}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验淀粉是否发生水解,将淀粉与稀硫酸溶液共热,冷却后,取上层水溶液,用NaOH中和稀硫酸后,再加入Cu(OH)2悬浊液,加热,观察是否产生砖红色沉淀 | |
| B. | 检验Fe(NO3)2晶体是否已氧化变质,将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液,观察溶液是否变血红色 | |
| C. | 在酸、碱中和滴定终点时不慎滴入过量标准溶液,可用装有待测液的滴定管再滴入一定量溶液进行调整 | |
| D. | 实验室制备氢氧化亚铁,滴加氢氧化钠溶液时应将胶头滴管插入硫酸亚铁溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 用试管加热碳酸氢钠固体时使试管口竖直向上 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 蒸馏时应先向冷凝管中通入冷凝水再加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 纯净物 | 纯硫酸 | 冰醋酸 | 水玻璃 | 胆矾 |
| 混合物 | 水煤气 | 福尔马林 | 冰水混合物 | 漂白粉 |
| 弱电解质 | 氨水 | 氟化氢 | 氨 | 水 |
| 非电解质 | 干冰 | 乙醇 | 三氧化硫 | 氯气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x+y>3 | |
| B. | 反应速率加快,活化分子百分数增加 | |
| C. | A的转化率减小,体积分数增大 | |
| D. | 平衡正向移动,平衡常数增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com