
 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: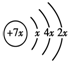 ,x=2,故A为Si元素,A、B、C同周期,即处于第三周期,B是同周期除稀有气体外半径最大的元素,B为Na元素,C的最外层有三个成单电子,外围电子排布为3s23p3,故C为P元素,C、D同主族,故D为N元素,E是过渡元素,其原子外围电子排布式为3d64s2,故E为Fe元素.
,x=2,故A为Si元素,A、B、C同周期,即处于第三周期,B是同周期除稀有气体外半径最大的元素,B为Na元素,C的最外层有三个成单电子,外围电子排布为3s23p3,故C为P元素,C、D同主族,故D为N元素,E是过渡元素,其原子外围电子排布式为3d64s2,故E为Fe元素. ,x=2,故A为Si元素,A、B、C同周期,即处于第三周期,B是同周期除稀有气体外半径最大的元素,B为Na元素,C的最外层有三个成单电子,外围电子排布为3s23p3,故C为P元素,C、D同主族,故D为N元素,E是过渡元素,其原子外围电子排布式为3d64s2,故E为Fe元素,则:
,x=2,故A为Si元素,A、B、C同周期,即处于第三周期,B是同周期除稀有气体外半径最大的元素,B为Na元素,C的最外层有三个成单电子,外围电子排布为3s23p3,故C为P元素,C、D同主族,故D为N元素,E是过渡元素,其原子外围电子排布式为3d64s2,故E为Fe元素,则: ,
, ;
; ,
, .
.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ?mol-1 | 436 | 391 | 945 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
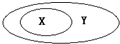 X、Y代表两组概念,其关系如下图,下列选项不满足相应关系的是( )
X、Y代表两组概念,其关系如下图,下列选项不满足相应关系的是( )| 选项 | X | Y |
| A | 氢键 | 化学键 |
| B | SO2 | 漂白性物质 |
| C | 油脂 | 酯 |
| D | 置换反应 | 氧化还原反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2S+2HNO3═S↓+2NO2↑+2H2O | ||||
| B、3FeO+10HNO3═3Fe(NO3)3+5H2O+NO↑ | ||||
C、4HNO3
| ||||
| D、3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com