
| A、Cu | B、Na | C、Al | D、Fe |
| m |
| n |
| 7.1g |
| 71g/mol |
| 6.4g |
| 0.1mol |


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3-C-18OHO和CH3CH2OH |
| B、CH3-C-18OHO和CH3CH2-18OH |
| C、CH3-C-18OH18O和CH3CH2-18OH |
| D、CH3-C-OHO和CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 难溶电解质 | AgI | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp(25℃) | 8.3×10-12 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-26 |
| A、氢氧化钠 | B、硫化钠 |
| C、碘化钾 | D、氢氧化钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、被还原的HNO3不可能是
| ||
B、溶液中剩余的n(NO3-)≤(0.4-
| ||
| C、溶液中不可能同时存在Fe2+、Fe3+、Cu2+ | ||
| D、被还原的硝酸为0.8a mol时,则溶液中一定含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
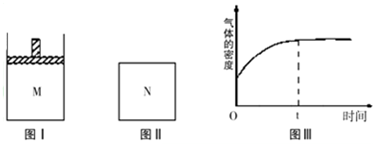
| A、x=2 |
| B、若N中气体的密度如图Ⅲ所示,则A、B只有一种是气态 |
| C、A为气体,B为非气体,则平衡时M、N中C的物质的量相等 |
| D、若A、B均为气体,平衡时M中A的转化率小于N中A的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
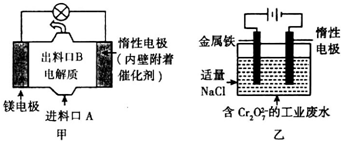
| A、图甲中发生的还原反应是Mg2++ClO-+H2O+2e-═Cl-+Mg(OH2)↓ |
| B、图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| C、图乙电解池中,若有0.084g阳极材料参与反应,则阴极会有336mL的气体产生 |
| D、若图甲燃料电池消耗3.6g镁产生的电量用以图乙废水处理,理论上可产生10.7g氢氧化铁沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
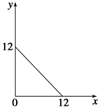 某温度(T℃)下的溶液中,c(H+)=10-x mol?L-1,c(OH-)=10-y mol?L-1,x与y的关系如图所示,请回答下列问题:
某温度(T℃)下的溶液中,c(H+)=10-x mol?L-1,c(OH-)=10-y mol?L-1,x与y的关系如图所示,请回答下列问题:| 实验序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
| 甲 | 乙 | 丙 | 丁 | |
| 0.1mol?L-1 Ba(OH)2溶液体积/mL | 10 | 10 | 10 | 10 |
| 0.1mol?L-1 NaHSO4溶液体积/mL | 5 | 10 | 15 | 20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一.莽草酸是A的一种异构体.A的结构简式如下:
莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一.莽草酸是A的一种异构体.A的结构简式如下: -COOH),其反应类型是
-COOH),其反应类型是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com