
| A、等物质的量浓度的下列溶液中,①NH4Cl②NH4Al(SO4)2③CH3COONH4④NH3?H2O,c(NH4+)由大到小的顺序是:②>①>③>④ |
| B、室温下,向0.01mol?L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| C、向0.2mol?L-1NaHCO3溶液中加如等体积0.1mol?L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、对于反应N2H4(l)=N2(g)+2H2(g)△H=-50.6kJ?mol-1在任何温度下都能自发进行 |


科目:高中化学 来源: 题型:

| A、容器I、Ⅲ中平衡常数相同 |
| B、容器Ⅱ、Ⅲ中正反应速率相同 |
| C、容器Ⅱ、Ⅲ中的反应达平衡时,SO3的体积分数:Ⅱ>Ⅲ |
| D、容器 I中SO2的转化率与容器 II中SO3的转化率之和小于1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油裂化得到的汽油是纯净物 |
| B、天然气是一种较为清洁的化石燃料 |
| C、石油产品都可用于聚合反应 |
| D、水煤气是指煤气中含有一定量的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
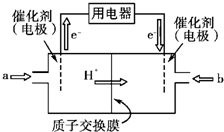 开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图所示:通入a气体的电极是原电池的
开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图所示:通入a气体的电极是原电池的查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.l mol?L-1的氨水溶液中:Na+、NH4+、NO3-、CO32- |
| B、0.1 mol?L-1的盐酸溶液中:K+、[Ag(NH3)2]+、Cl-、NO3- |
| C、使蓝色石蕊试纸变红的溶液中:CO32-、SO32-、Na+、K+ |
| D、由永电离出的c(H+)=1×l0-12 mol?L-l的溶液中:Fe2+、ClO-、K+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2S?2H++S2- |
| B、NaHCO3═Na++H++CO32- |
| C、K2SO4═2K++SO42- |
| D、NH3?H2O═NH4++H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com