
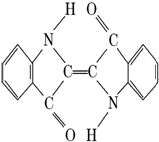
 历史上最早应用的还原性染料是靛蓝,其结构简式如右图,下列关于靛蓝的叙述中错误的是( )
历史上最早应用的还原性染料是靛蓝,其结构简式如右图,下列关于靛蓝的叙述中错误的是( )| A. | 靛蓝由碳、氢、氧、氮四种元素组成 | B. | 它的分子式是C16H10N2O2 | ||
| C. | 该物质属于芳香化合物 | D. | 它含有碳碳双键和酯基 |
分析 A.由靛蓝的结构简式可知,靛蓝由碳、氢、氧、氮四种元素组成;
B.由结构可知,分子中含有16个C原子、10个H原子、2个N原子、2个O原子;
C.含有苯环的化合物属于芳香族化合物;
D.由结构可知,靛蓝不含酯基.
解答 解:A.由靛蓝的结构简式可知,靛蓝由碳、氢、氧、氮四种元素组成,故A正确;
B.由结构可知,分子中含有16个C原子、10个H原子、2个N原子、2个O原子,分子式为:C16H10N2O2,故B正确;
C.靛蓝含有苯环,属于芳香族化合物,故C正确;
D.由结构可知,靛蓝不含酯基,故D错误.
故选:D.
点评 本题考查有机物的结构与性质,注意把握官能团与物质类别的关系,注重基础知识的考查和知识迁移应用,侧重概念的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式:${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{C}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$ | |
| B. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl | |
| C. | NH4Cl的电子式: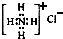 | |
| D. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
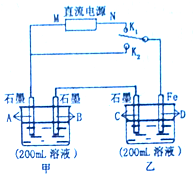 如图所示,甲、乙两个烧杯中的溶液中溶质离子分别由Na+、Cu2+、Cl-、SO42-四种离子中的一种阳离子和一种阴离子组成.(每种离子只能选用一次)
如图所示,甲、乙两个烧杯中的溶液中溶质离子分别由Na+、Cu2+、Cl-、SO42-四种离子中的一种阳离子和一种阴离子组成.(每种离子只能选用一次)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜锌原电池中铜是正极 | |
| B. | 铁壳船底部镶嵌铜块,铜块更易被腐蚀 | |
| C. | 用电解法精炼粗铜时粗铜作阳极 | |
| D. | 在镀件上镀铜是可用金属铜作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯与氢气可以发生加成反应 | B. | 甲苯燃烧带有浓厚的黑烟 | ||
| C. | 甲苯能使酸性高锰酸钾溶液褪色 | D. | 甲苯硝化生成三硝基甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60s时X的平均反应速率为0.02mol/L | |
| B. | 将容器容积变为20L,Z的新平衡浓度将等于原平衡浓度的$\frac{1}{2}$ | |
| C. | 若温度和体积不变,往容器内增加1molX,Y的转化率将增大 | |
| D. | 若升高温度,X的体积分数增大,则正反应的△H>0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com