

 ��
�� ���� ��Ԫ�������ڱ���λ�ã���֪��ΪH����ΪN����ΪO����ΪF����ΪNa����ΪAl����ΪS����ΪCl����ΪAr����ΪK��
��1��ͬ����������ҷǽ�������ǿ��ͬ�������϶��·ǽ����Լ�����ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ϡ������ԭ�������Ϊ�ȶ��ṹ����ѧ��������ã�
��2������������Ӧˮ������������ǿ���Ǹ����ᣬ����Ԫ����K�Ľ�������ǿ�����������صļ�����ǿ��
��3����̬�⻯������������������Ӧ��ˮ���ﷴӦ�����Σ�Ӧ�ǰ��������ᷴӦ��������泥�
��4������������������������ݺ͢ߵ�����������Ӧ��ˮ����ֱ�ΪNaOH�����ᣬ�����������������Ʒ�Ӧ����ƫ��������ˮ���������������ᷴӦ������������ˮ��
��5��Ԫ��ԭ�ӵõ�������Խǿ�����⻯��Խ�ȶ�����ۺ����������Խǿ�������ӵĻ�ԭ��Խ����
��6��a��ͬ�������϶��·ǽ����Լ�����
b�����ӽṹ��������ƣ���Է�������Խ���۵�Խ�ߣ�
c��HF����֮�����������е���ߣ�
��7���١��ۡ��ݡ����е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����Թ��ۼ��Ļ�������NaOH��NaClO�ȣ�
��� �⣺��Ԫ�������ڱ���λ�ã���֪��ΪH����ΪN����ΪO����ΪF����ΪNa����ΪAl����ΪS����ΪCl����ΪAr����ΪK��
��1��ͬ����������ҷǽ�������ǿ��ͬ�������϶��·ǽ����Լ�����������Ԫ����FԪ�صķǽ�������ǿ��ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶��������Ԫ����K��ԭ�Ӱ뾶���ϡ������Arԭ�������Ϊ�ȶ��ṹ����ѧ��������ã�
�ʴ�Ϊ���ܣ��⣻�
��2������������Ӧˮ������������ǿ���Ǹ����ᣬ�仯ѧʽΪHClO4������Ԫ����K�Ľ�������ǿ����KOH�ļ�����ǿ��
�ʴ�Ϊ��HClO4��KOH��
��3����̬�⻯������������������Ӧ��ˮ���ﷴӦ�����Σ�Ӧ�ǰ��������ᷴӦ��������泥���Ӧ����ʽΪ��NH3+HNO3�TNH4NO3��
�ʴ�Ϊ��NH3+HNO3�TNH4NO3��
��4������������������������ݺ͢ߵ�����������Ӧ��ˮ����ֱ�ΪNaOH�����ᣬ�����������������Ʒ�Ӧ����ƫ��������ˮ����Ӧ���ӷ���ʽΪ��Al��OH��3+OH-�TAlO2-+2H2O���������������ᷴӦ������������ˮ����Ӧ���ӷ���ʽΪ��Al��OH��3+3H+�TAl3++3H2O��
�ʴ�Ϊ��Al��OH��3+OH-�TAlO2-+2H2O��Al��OH��3+3H+�TAl3++3H2O��
��5���ٺ�������ȶ��Բ��ܱȽϷǽ���Ԫ�صõ������������Ը����⻯���ȶ����жϣ��ʴ���
�ڸ������DZ������ǿ���ᣬ˵����Ԫ�طǽ����Ա����ǿ������ԭ�ӵõ���������ǿ������ȷ��
��S2-��Cl-�ױ�������˵����Ԫ�طǽ����Ա����ǿ������ԭ�ӵõ���������ǿ������ȷ��
��HC1��H2S�ȶ���˵����ԭ�ӵõ���������ǿ������ȷ��
��ͭ�������Ӧ����Ũ�����ܷ�Ӧ������˵����ԭ�ӵõ���������ǿ���ʴ���
��ѡ���ڢۢܣ�
��6��a��ͬ�������϶���ԭ�Ӱ뾶����ԭ�Ӻ˶Ժ�����������������ǽ����Լ�������F��Cl��Br�ķǽ����Խ�������a��ȷ��
b��F2��Cl2��Br2�Ľṹ���ƣ���Է������������������۵��������ߣ���b����
c��HBr��HI�ṹ���ƣ�������Է��������������е����ߣ�HF����֮�����������е���ߣ���c����
��ѡ��a��
��7���١��ۡ��ݡ����е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����Թ��ۼ��Ļ�������NaOH��NaClO�ȣ�NaOH�ĵ���ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼��Ԫ�����ڱ���Ԫ�������ɣ���������Ԫ�������ɱ��Ľṹ������Ԫ�������ɣ�����Ԫ�ؽ����ԡ��ǽ�����ǿ���ȽϷ����������ڻ���֪ʶ�Ĺ��̣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �¶�/�� | 400 | 500 | 600 |
| SO2ת����/% | 99.2 | 93.5 | 73.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
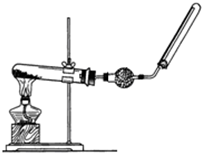 ʵ������������ͼ��ʾ��װ����ȡ���ռ�����İ�����
ʵ������������ͼ��ʾ��װ����ȡ���ռ�����İ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ����֪Ũ��NaOH��Һ�ζ�δ֪Ũ�����ᣬ�ζ��յ�ʱ�����ӿ̶��ߣ���������Ũ��ƫС | |
| B�� | ������������ͭ����Һ���Լ������ᡢ�����Ǻ͵���������Һ | |
| C�� | ͨ�����ò������ݵĿ��������Ƚϲ�ͬ������Na2S2O3��Һ��ϡ����ķ�Ӧ���� | |
| D�� | ��ǿ���ǿ�ʴ����ʱ��Ӧ���ô���ˮ��ϴ������2%������Һ��������Һϴ�������ˮ��ϴ�������������һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
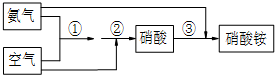
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
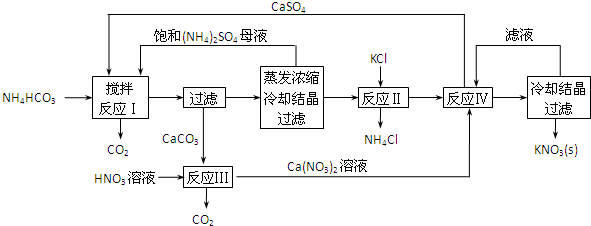
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
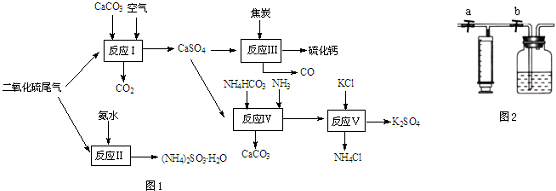
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | пƬ�ܽ���32.5 g | B�� | пƬ����32.5 g | ||
| C�� | ͭƬ������lgH2 | D�� | ͭƬ������1molH2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com