
| A. | 5min内D的平均反应速率是0.2mol/(L•min) | |
| B. | 3υA=2υD | |
| C. | x的值是2 | |
| D. | A的起始物质的量为1.5mol |
分析 经测定5min内C的平均反应速率是0.1mol/(L•min),同时生成1mol D,v(D)=$\frac{\frac{1mol}{2L}}{5min}$=0.1mol/(L•min),由速率之比等于化学计量数之比可知,x=2,A、B的起始物质的量及5min后的物质的量不能确定,以此来解答.
解答 解:A.v(D)=$\frac{\frac{1mol}{2L}}{5min}$=0.1mol/(L•min),故A错误;
B.由速率之比等于化学计量数之比可知,$\frac{{v}_{A}}{{v}_{D}}$=$\frac{3}{2}$,则2υA=3υD,故B错误;
C.v(C)=0.1mol/(L•min),v(D)=0.1mol/(L•min),由速率之比等于化学计量数之比可知,x=2,故C正确;
D.由题中信息只能计算转化的A的物质的量,不能确定A的起始物质的量,故D错误;
故选C.
点评 本题考查化学平衡的计算,为高频考点,把握化学反应速率的计算公式、速率与化学计量数的关系为解答的关键,侧重分析与计算能力的考查,注意起始物质的量不能确定,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题


 +CH3CH2OH$\stackrel{H+}{→}$
+CH3CH2OH$\stackrel{H+}{→}$ +H2O,
+H2O, ;
; ,则H的结构简式是
,则H的结构简式是 .高聚物L由H通过肽键连接而成,写出生成L的方程式n
.高聚物L由H通过肽键连接而成,写出生成L的方程式n →nH2O+
→nH2O+ (或
(或 ),.
),.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Y 表示的化学反应速率为0.005 mol/(L•s) | |
| B. | 将容器体积变为20 L,Z的平衡浓度变为原来的$\frac{1}{2}$ | |
| C. | 若升高温度Y的转化率减小,则正反应为放热反应 | |
| D. | 达到平衡时,Y与Z的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
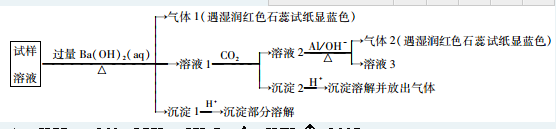

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同周期元素的原子电子层数相同 | |
| B. | (长式)元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的 | |
| C. | 最外层电子数相同的元素都是同一族的元素 | |
| D. | 同一主族元素的原子最外层电子数一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
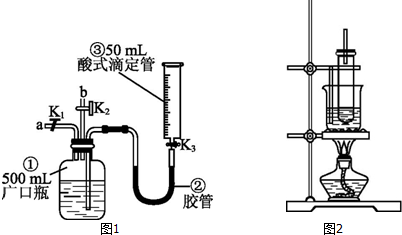
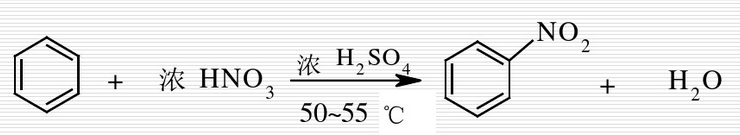 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷 | |
| B. | 用NaOH溶液可以区分HCOOCH3和HCOOCH2CH3 | |
| C. | 用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 | |
| D. | 油脂在酸性或碱性条件下均能发生水解反应,且产物相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com