
分析 化学反应中,化学键断裂吸收能量,形成新化学键放出能量,根据方程式计算,化学反应中,反应物的总能量大于生成物的总能量,反应放热,反之吸热,以此计算反应热并判断吸热还是放热.
解答 解:拆1molH-H键、1molN≡N、1molN-H键分别需要吸收的能量为436kJ、946kJ、391kJ,在反应N2+3H2?2NH3中,断裂3mol H-H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,消耗1molN2生成2molNH3,共形成6molN-H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ-2254kJ=92kJ,所以生成1mol NH3放出热量为46KJ;1molH2生成$\frac{2}{3}$molNH3,放出热量为$\frac{2}{3}$×46KJ=$\frac{92}{3}$kJ,
故答案为:放出;46;放出;$\frac{92}{3}$;放出;92.
点评 本题考查反应热的计算,题目难度不大,注意把握从键能的角度计算反应热的方法.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 现欲用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
现欲用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 硬度比生铁低 | B. | 在潮湿空气中放置不易生锈 | ||
| C. | 可溶在稀H2S04中 | D. | 熔点比生铁低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
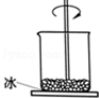 如图,小烧杯放在一块沾有水的玻璃片上,加入NH4Cl固体与氢氧化钡晶体[Ba(OH)2•8H2O],并用玻璃棒搅拌,玻璃片上的水结成了冰.由此可推断( )
如图,小烧杯放在一块沾有水的玻璃片上,加入NH4Cl固体与氢氧化钡晶体[Ba(OH)2•8H2O],并用玻璃棒搅拌,玻璃片上的水结成了冰.由此可推断( )| A. | 该反应中,化学能转变成热能 | |
| B. | 反应物的总能量低于生成物的总能量 | |
| C. | 氯化铵与氢氧化钡的反应为放热反应 | |
| D. | 反应的热化学方程式为:2NH4Cl+Ba(OH)2═BaCl2+2NH3•H2O△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
| A. | 元素②与元素③处于同一周期 | |
| B. | 元素④的原子序数小于元素⑦的 | |
| C. | 元素⑧的还原性比元素⑥的强 | |
| D. | 元素⑤的最高价氧化物对应水化物的酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 在某有机物A的分子中,具有酚羟基、醇羟基、羧基等官能团,其结构简式如图.
在某有机物A的分子中,具有酚羟基、醇羟基、羧基等官能团,其结构简式如图.

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
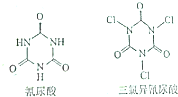 NA表示阿伏加德罗常数的值,下列说法中正确的有几项( )
NA表示阿伏加德罗常数的值,下列说法中正确的有几项( )| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B、C、D 形成的简单离子半径依次增大 | |
| B. | B、C 形成的化合物只含有离子键 | |
| C. | A、C、D 形成的化合物CDA4,属于离子化合物,有较强的还原性 | |
| D. | A、B、C 形成的化合物与B、C、D 形成的化合物可以发生化学反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com