
【题目】【成都市2017届第二次模拟考试】前四周期元素A、B、C、D、E的原子序数依次增大,A的质子数等于周期数,B与C的 P轨道均有三个成单电子,D的最高正价与最低负价代数和为4,E的最外层只有一个电子, 内层轨道处于全充满状态。试回答下列问题。
(1)基态E原子的电子排布式为_________;C和D的第一电离能较大的________(填元素符号)。
(2)DO32-中D原子的杂化类型为_________;A、D和氧元素组成的液态化合物A2DO4中存在的作用力有_____________。
(3)结构式为A—B=B—A的分子中σ键和π键的数目比为________;B2分子和NO+离子互为等离子体,则NO+的电子式为___________。
(4)向EDO4溶液中加入过量稀氨水,其化学方程式为______;产物中阳离子的配体是______(填化学式)。
(5)D(黑球)和E(白球)形成某种晶体的晶胞如图所示。已知该晶体的晶胞边长为516Pm,则黑球和白球之间最近距离为________pm(精确到0.1,已知![]() =1.732)若ED中D2-被O2-代替,形成的晶体只能采取NaCl型堆积,试从晶体结构分析其不同及原因__________。
=1.732)若ED中D2-被O2-代替,形成的晶体只能采取NaCl型堆积,试从晶体结构分析其不同及原因__________。

【答案】1s22s22p63s23p63d104s1或[Ar]3d104s1 P sp2 氢键、范徳华力、共价键 3∶1
![]() CuSO4+4 NH3·H2O ==[Cu(NH3)4]SO4+4 H2O NH3 223.4 两种晶体中离子的配位数不同。由于r(O2-) < r(S2-),r+ /r-的值增大,晶体中离子的配位数由4增至6,导致晶体堆积方式不同。
CuSO4+4 NH3·H2O ==[Cu(NH3)4]SO4+4 H2O NH3 223.4 两种晶体中离子的配位数不同。由于r(O2-) < r(S2-),r+ /r-的值增大,晶体中离子的配位数由4增至6,导致晶体堆积方式不同。
【解析】本题考查选修三《物质结构与性质》,A的质子数等于周期数,则A为H,B与C的p轨道均有三个成单电子,说明B和C属于同主族,即分别属于N和P,D的最高正价与最低负价的代数和为4,则D为S,E的最外层只有一个电子,且内层全充满,因此E为Cu, (1)Cu位于第四周期第IB族,因此电子排布式为:1s22s22p63s23p63d104s1或[Ar]3d104s1 ;P和S属于同周期,同周期第一电离能从左向右增强,但IIA>IIIA、VA>VIA,因此第一电离能P>S;(2)DO32-为SO32-,其中S有3个σ键,孤电子对数为(6+2-3×2)/2=1,价层电子对数为4,即SO32-中S的杂化类型为sp3;组成的化合物是H2SO4,含有的作用力是共价键、范德华力、氢键;(3)成键原子之间只能有1个σ键,双键中有1个π键,因此H-N=N-H中σ键和π键的比值为3:1;等电子体的结构相似,N2的结构式为![]() ,因此NO+的电子式为
,因此NO+的电子式为![]() ;(4)EDO4的化学式为CuSO4,与过量的氨水发生络合反应,反应方程式为:CuSO4+4NH3·H2O=[Cu(NH3)4]SO4+4H2O,Cu2+提供空轨道,NH3提供孤电子对,因此NH3是配体;(5)根据晶胞的结构,黑球和白球之间最近的距离是体对角线的1/4,即为
;(4)EDO4的化学式为CuSO4,与过量的氨水发生络合反应,反应方程式为:CuSO4+4NH3·H2O=[Cu(NH3)4]SO4+4H2O,Cu2+提供空轨道,NH3提供孤电子对,因此NH3是配体;(5)根据晶胞的结构,黑球和白球之间最近的距离是体对角线的1/4,即为![]() (a为晶胞的边长),代入数值,解得为223.4pm,两种晶体中离子的配位数不同。由于r(O2-)<r(S2-),r+/r-的值增大,晶体中离子的配位数由4增至6,导致晶体堆积方式不同。
(a为晶胞的边长),代入数值,解得为223.4pm,两种晶体中离子的配位数不同。由于r(O2-)<r(S2-),r+/r-的值增大,晶体中离子的配位数由4增至6,导致晶体堆积方式不同。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】醋硝香豆素是一种治疗心脑血管疾病的药物,能阻碍血栓扩展,醋硝香豆素可以通过以下方法合成(部分反应条件省略)。

已知:
回答以下问题:
(1)A物质的名称是__________。
(2)反应类型:①___________;②_________。
(3)写出C的结构简式__________。
(4)写出反应③的化学反应方程式:__________________________________。
⑸分子结构中只含有一个环,且同时符合下列条件的G的同分异构体共有_____种。
可与氯化铁溶液发生显色反应; ② 可与碳酸氢钠溶液反应生成二氧化碳气体。
请写写请写出在核磁共振氢谱中峰面积之比为2:2:1:1的同分异构体的结构简式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完全沉淀相同体积的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗相同浓度的AgNO3溶液的体积之比为3:2:1,则NaCl、MgCl2、AlCl3溶液的物质的量浓度之比为( )
A. 1:2:3 B. 3:2:1 C. 6:3:2 D. 9:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质鉴别所用试剂不正确的是( )
A.乙醇与乙酸用CaCO3固体B.乙醇和乙醛用酸性高锰酸钾溶液
C.苯和乙酸用水D.乙烯与乙烷用酸性高锰酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【广州市2017届4月综合测试(二)】硼及其化合物应用广泛。回答下列问题:
(1)基态B原子的价电子轨道表达式为________,其第一电离能比Be ________(填“大”或“小”)。
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________,写出一种与氨硼烷互为等电子体的分子________(填化学式)。

(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图a。
① B原子的杂化方式为________。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:________。
② 路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸:________。
(4)立方氮化硼(BN)是特殊的耐磨和切削材料,其晶胞结构与金刚石相似,如图b所示。
① 与氮原子直接连接的硼原子构成的几何形状为________。硼原子和氮原子所连接的最小环为________元环。
② 晶胞有两个基本要素:
原子坐标参数,表示晶胞内部各原子的相对位置。如图b所示,其中原子坐标参数X为(0,0,0),Y原子的坐标参数为(1/2,0,1/2),则Z原子的坐标参数为________。
晶胞参数,描述晶胞的大小和形状。已知立方氮化硼的密度为d gcm-3,阿伏加德罗常数值为NA,则晶胞参数a=________nm。(列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【山西省实验中学2017届下学期模拟热身】[化学―选修3:物质结构与性质]
研究物质的微观结构,有助于人们理解物质变化的本质。请根据已学习的物质结构知识,回答下列问题:
(1)基态Mn原子的价电子排布式为___,气态Mn2+再失去l个电子比Fe2+再失去1个电子更难,其原因是________。
(2)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有_____。写出难溶物溶于氨水时的离子方程式__________。实验过程中加入C2H5OH 后可观察到析出深蓝色Cu(NH3)4SO4·5H2O晶体。实验中所加C2H5OH 的作用是______。
(3)HClO2、HClO3为氯元素的含氧酸,试推测ClO2-的空间结构:________;HClO3分子中,Cl原子的杂化方式为______;两种酸酸性较强的是_______.
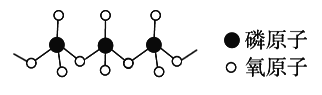
(4)多磷酸盐的酸根阴离子是由两个或两个以上磷氧四面体通过共用角顶氧原子而连接起来的,部分结构如图所示,多磷酸根离子的通式为______。(磷原子数目用n表示)
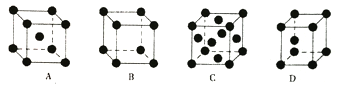
(5)金属Pt采用“…ABCABC…”型堆积方式,抽出一个晶胞,其正确的是________。
已知金属Pt的密度为21.4 g/cm3,则Pt原子半径的计算式为______pm (只列式,不必计算结果,Pt的相对原子质量为M,阿伏加德罗常数为6.02×1023mol-1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA 代表阿伏加德罗常数的值,下列说法正确的是
A. 1 L 0.1 mol·![]() NH4Cl溶液中,
NH4Cl溶液中, ![]() 的数量为0.1
的数量为0.1![]()
B. 标准状况下,2.24 L N2和O2的混合气体中分子数为0.2![]()
C. 1molCl 2 完全反应,转移的电子数一定为 2N A
D. 14 g 乙烯和丙烯混合气体中的氢原子数为 2N A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【衡阳市2017届下学期第三次联考】甲乙两实验小组同学对铁及其化合物的性质进行如下探究:
I.甲组同学利用如图装置探究过量铁粉与浓H2SO4反应产生的气体成分。

(1)组装好实验仪器后,接下来的实验操作是____________________;
(2)B中观察到品红溶液褪色,D中收集到VmL水,说明A中反应产生气体的成分
是______________________。
II.乙组同学对反应后圆底烧瓶溶液中所含金属离子进行探究。
(3)铁与浓H2SO4的反应过程中必有Fe3+生成。取适量反应后的溶液,加入少量KSCN溶液,不变红色。原因是_______________(用离子方程式表示)。
(4)取适量反应后的溶液,加人少量酸性高锰酸钾溶液,溶液褪色。该反应原理的离子方程式为 _______________________。
(5)取少量反应后的溶液,先滴加少量新制氯水,再滴加KSCN溶液,呈现血红色,继续滴加过量新制氯水,红色褪去。
①分析其可能的原因是:
A.溶液中Fe3+被氧化成更髙价;
B.____________________________;
C.______________________。
②请选用下列合适的化学试剂,验证结论A是否正确。0.lmol/L FeCl3溶液、lmol/L FeCl2溶液、KSCN溶液、新制氯水、一定浓度的H2O2溶液。
操作、现象及相关结论为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。其中一种合成路线如下:

已知:
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4种氢,且峰面积之比为1︰2︰2︰1。
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平。
③![]()
回答以下问题:
(1)A中含有的官能团名称是_________________________________。
(2)写出有机反应类型B→C__________,F→G_________,I→J_________。
(3)写出F生成G的化学方程式____________________________________。
(4)写出J的结构简式__________________________________。
(5)E的同分异构体有多种,写出所有符合以下要求的E的同分异构体的结构简式_____________。
①FeCl3溶液发生显色反应 ②能发生银镜反应
③苯环上只有两个对位取代基 ④能发生水解反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com