
【题目】“绿水青山就是金山银山”,研究NO2、NO、CO、S02等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)已知: ①NO2+CO![]() CO2+NO该反应的平衡常数为K1(下同),每1mol下列物质分解为气态基态原子吸收的能量分别为
CO2+NO该反应的平衡常数为K1(下同),每1mol下列物质分解为气态基态原子吸收的能量分别为
NO2 | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
②N2(g)+O2(g) ![]() 2NO(g) △H=+179.5kJ/mol K2
2NO(g) △H=+179.5kJ/mol K2
③2NO(g)+O2(g)![]() 2NO2(g) △H=-112.3kJ/mol K3
2NO2(g) △H=-112.3kJ/mol K3
写出NO与CO反应生成无污染气体的热化学方程式____________________________________,该热化学方程式的平衡常数K=_________(用K1、K2、K3表示)。
(2)在体积可变的恒压(p总)密闭容器中充入1molCO2 与足量的碳,让其发生反应: C(s)+ CO2(g)![]() 2CO(g) △H>0。平衡时,体系中气体体积分数与温度的关系如下图所示。
2CO(g) △H>0。平衡时,体系中气体体积分数与温度的关系如下图所示。
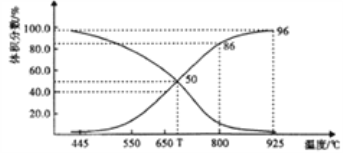
①T℃时,在容器中若充入稀有气体,v(正)___v(逆)(填“>”“<”或“="),平衡______移动(填“正向”“逆向”或“不”。下同);若充入等体积的CO2 和CO,平衡________移动。
②CO体积分数为40%时,CO2 的转化率为_______。
③已知:气体分压(p分)=气体总压×体积分数。用平衡分压代替平衡浓度表示平衡Kp常数的表达式为__________;925℃时,Kp=______(用含p总的代数式表示)。
(3)直接排放含SO2 的烟气会形成酸雨,危害环境。可用NaOH吸收,所得含硫各微粒(H2SO3、HSO3-和SO32-)存在于反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。

①若是0.1mol/LNaOH 反应后的溶液,测得溶液的pH=8时,溶液中各离子浓度由大到小的顺序是______________。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2 溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因_______________________________________________。
【答案】 2NO(g) +2CO(g)![]() N2(g) +2CO2(g) △H=-759.8 kJ/mol
N2(g) +2CO2(g) △H=-759.8 kJ/mol ![]() > 正向 不 25%
> 正向 不 25% ![]() 23.04p总 c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+) 因为亚硫酸氢根离子存在电离平衡HSO3-
23.04p总 c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+) 因为亚硫酸氢根离子存在电离平衡HSO3-![]() H++SO32-,加入氯化钙后,Ca2++SO32-=CaSO3↓,使平衡正向移动,氢离子浓度增大,pH减小
H++SO32-,加入氯化钙后,Ca2++SO32-=CaSO3↓,使平衡正向移动,氢离子浓度增大,pH减小
【解析】(1)由已知,反应①的△H=(812+1076-1490-632)kJ/mol=-234kJ/mol,根据盖斯定律,①×2+③-②得:2NO2(g)+2CO(g)![]() N2(g)+2CO2(g),△H=[-234×2+(-112.3)-179.5]kJ/mol=-759.8kJ/mol;当总反应式相加时平衡常数相乘,相减时平衡常数相除,成倍时平衡常数为幂,所以平衡常数K=
N2(g)+2CO2(g),△H=[-234×2+(-112.3)-179.5]kJ/mol=-759.8kJ/mol;当总反应式相加时平衡常数相乘,相减时平衡常数相除,成倍时平衡常数为幂,所以平衡常数K=![]() 。
。
(2)①该反应正向为气体分子数减小反应,恒温恒压时充入稀有气体,对该反应来说相当于减压,v(正)>v(逆),平衡正向移动。
②设CO2的转化率为α,由已知列三段式得:

![]() ×100%=40%,解得α=25%。
×100%=40%,解得α=25%。
③用平衡浓度表示该反应化学平衡常数表达式为K= ,所以若用平衡分压代替平衡浓度表示平衡常数的表达式为Kp=
,所以若用平衡分压代替平衡浓度表示平衡常数的表达式为Kp= ;由图可得,925℃时CO体积分数为96%,分压为96%×p总,CO2体积分数为4%,分压为4%×p总,所以Kp=
;由图可得,925℃时CO体积分数为96%,分压为96%×p总,CO2体积分数为4%,分压为4%×p总,所以Kp= =
= =23.04p总。
=23.04p总。
(3)①由图可得,pH=8时溶液中溶质主要为Na2SO3和NaHSO3,c(SO32-)>c(HSO3-),溶液中的主要离子为:Na+、SO32-、HSO3-,次要离子为OH-、H+,所以各离子浓度由大到小的顺序是:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)。②NaHSO3溶液中HSO3-存在电离平衡HSO3-![]() H++SO32-,加入氯化钙后,Ca2++SO32-=CaSO3↓,使电离平衡正向移动,氢离子浓度增大,所以pH降低。
H++SO32-,加入氯化钙后,Ca2++SO32-=CaSO3↓,使电离平衡正向移动,氢离子浓度增大,所以pH降低。


科目:高中化学 来源: 题型:
【题目】已知:在常温下,苯(C6H6)为一种无色、透明的液体,毒性较高,易挥发,易燃,有腐蚀性,沸点为80.1℃,难溶于水,易溶于有机溶剂,可作为有机溶剂;碘(I2)为紫黑色晶体,易升华,易凝华,熔点113.5℃,沸点184.3℃,加热时碘升华为紫色蒸气,冷却后凝华成紫黑色固体。实验室常用苯来提取碘水中的碘,具体操作如下:

①向碘的水溶液中加入萃取剂苯,转移到分液漏斗中,塞上玻璃塞,充分振荡放气后(如图1);
②将分液漏斗置于铁架台的铁圈上静置(如图2);
③当分液漏斗中的液体分成清晰的两层后,经“合适的操作”将两层液体进行分离;
④将分离出的碘和苯的混合液转移到仪器A中,加入少量沸石进行蒸馏以分离苯和碘(如图3)。
请回答下列问题:
(1)分液漏斗在使用前必须进行的操作是_______。
(2)步骤③中“合适的操作”的名称是________。
(3)步骤④中采用水浴加热而不直接加热的原因是________________;图3中有多处明显的错误:a.冷却水进出方向错误.b.___________________。
(4)锥形瓶置于冰水中的目的是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铅蓄电池的工作原理为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。

(1)A是铅蓄电池的________极,Cu电极是________极,放电过程中电解液的密度________(填“减小”“增大”或“不变”)。
(2)Ag电极的电极反应式是______________________________,该电极的电极产物共________g。
(3)Cu电极的电极反应式是______________________________,CuSO4溶液的浓度________(填“减小”“增大”或“不变”)
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示________。

a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题。
(1)CO可用于合成甲醇。在体积可变的密闭容器中充入4molCO和8molH2,在催化剂作用下合成甲醇:CO(g)+2H2(g)![]() CH3OH(g)(Ⅰ),平衡时CO的转化率与温度、压强的关系如下图所示:
CH3OH(g)(Ⅰ),平衡时CO的转化率与温度、压强的关系如下图所示:

①该反应的逆反应属于________反应;(填“吸热”或“放热”)。
②在0.1Mpa 、100℃的条件下,该反应达到平衡时容器体积为开始容器体积的_________倍。(结果保留两位小数点)
③在温度和容积不变的情况下,再向平衡体系中充入4molCO,达到平衡时CO转化率________(填“增大”,“不变”或“减小”),平衡常数K________(填“增大”,“不变”或“减小”)。
(2)在反应(Ⅰ)中需要用到H2做反应物,以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
①CH4(g)+ H2O(g)= CO(g)+3H2(g) △H=+206.2 kJ·mol-1
②CH4(g)+ CO2(g)= 2CO(g)+2H2(g) △H=+247.4 kJ·mol-1
则CH4和H2O(g)反应生成CO2和H2的热化学方程式为: 。
(3)在反应(Ⅰ)中制得的CH3OH 即可以做燃料,还可以与氧气组成碱性燃料电池,电解质溶液是20%~30%的KOH溶液。则该燃料电池放电时:负极的电极反应式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质,下列实验现象和结论一 致且正确的是
A. 加入有色布条,褪色,说明溶液中有 Cl2 存在
B. 溶液呈现黄绿色,且有刺激性气味,说明有 Cl2 存在
C. 先加入盐酸酸化,再加入硝酸银溶液产生白色沉淀,说明有 Cl-存在
D. 新制氯水放置数天后酸性将减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶A和盛有潮湿有色布条的广口瓶B,可观察到的现象是_________; 设计实验 A 的目的是_____;写出氯气与水反应的化学方程式:___________。

(2)在该实验中,装置还存缺陷,你认为还需加_____装置才能使实验符合要求,写出其反应的化学方程式_____。
(3)根据(2)中反应原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,化学反应方 程式为:_____。漂白粉溶于水后,受空气中的 CO2 作用, 即产生有漂白、杀菌作用的物质,化学反应方程式为:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】老师用下图所示装置为同学们做了一个兴趣实验。已知装置B、C、D中依次盛有紫色石蕊试液、足量的澄清石灰水和稀盐酸。小资料:HCl气体极易溶于水。

(1)打开A中的玻璃塞和活塞,B中实验现象是________________________。B中的现象不能说明二氧化碳与水反应的原因是________________________________________。
C中的化学反应的方程式是________________________________________________。
(2)一段时间后,关闭A中的活塞和玻璃塞,打开弹簧夹K2及E中的玻璃塞和活塞,待足量的过氧化氢溶液流入锥形瓶后,立即关闭E中的活塞,并用弹簧夹K2夹紧橡皮管。C中可能出现的现象是____________________________,解释C中呈现的现象的原因是______________________________________________________________________。
(3)将A中产生的气体通入过量的NaOH溶液中,为了确定反应后的溶液中含有NaOH 的实验方法为_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com