
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电时,负极质量增加 |
| B、充电时,应将外接直流电源的正极与蓄电池的铅电极相接 |
| C、放电时,正极反应为:PbO2+4H++SO42-+2e-=PbSO4+2H2O |
| D、铅蓄电池做电源电解Na2SO4溶液时,当有1mol O2产生时,消耗4mol H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4)(mol/L) | 0.20 | a | 0.10 | c | d | e |
| C(NO2)(mol/L) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
查看答案和解析>>
科目:高中化学 来源: 题型:
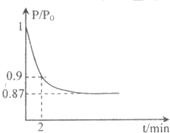 某实验小组模拟工业合成氨,利用合成的氨气验证氨气具有还原性实验.
某实验小组模拟工业合成氨,利用合成的氨气验证氨气具有还原性实验.| 催化剂 |
| 高温、高压 |
| P |
| P0 |
| 实验步骤 | 现象和结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.8克金属铝变为铝离子时失去的电子数目为0.1NA |
| B、1.8克818O2中所含的中子数目为NA |
| C、在常温常压下11.2升氯气所含的原子数目为NA |
| D、氧气的摩尔质量与NA个O2分子的质量相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com