
【题目】金属钠长时间露置于空气中,最终转化为什么产物?请写出主要反应的化学方程式__________。
【答案】Na2CO3;4Na+O2=2Na2O、Na2O+H2O=2NaOH、2NaOH+CO2=Na2CO3+H2O、Na2CO3+10H2O=Na2CO3·10H2O、Na2CO3·10H2O![]() Na2CO3+10H2O
Na2CO3+10H2O
【解析】
一般条件下,银白色金属(Na)![]() 表面变暗(生成Na2O)
表面变暗(生成Na2O)![]() 变为白色固体(生成NaOH)
变为白色固体(生成NaOH)![]() 表面形成溶液(NaOH潮解)
表面形成溶液(NaOH潮解)![]() 结块(形成Na2CO3·10H2O)
结块(形成Na2CO3·10H2O)![]() 最终变成白色粉末(生成Na2CO3);有关反应如下:4Na+O2=2Na2O,Na2O+H2O=2NaOH,2NaOH+CO2=Na2CO3+H2O,Na2CO3+10H2O=Na2CO3·10H2O,Na2CO3·10H2O
最终变成白色粉末(生成Na2CO3);有关反应如下:4Na+O2=2Na2O,Na2O+H2O=2NaOH,2NaOH+CO2=Na2CO3+H2O,Na2CO3+10H2O=Na2CO3·10H2O,Na2CO3·10H2O![]() Na2CO3+10H2O,
Na2CO3+10H2O,
故答案为:Na2CO3;4Na+O2=2Na2O、Na2O+H2O=2NaOH、2NaOH+CO2=Na2CO3+H2O、Na2CO3+10H2O=Na2CO3·10H2O、Na2CO3·10H2O![]() Na2CO3+10H2O。
Na2CO3+10H2O。


科目:高中化学 来源: 题型:
【题目】据有关媒体报道,美国华裔科学家叶军领导一个研究小组成功制造出全球最准确的时钟,两亿年误差不足一秒。它是一个锶原子钟,比铯原子喷泉钟准确得多,估计将可大大促进不同的电讯网络的发展,将使全球各地的船只导航变得更为准确。请根据锶、铯在元素周期表中的位置,推断下列内容:
(1)锶元素属于________(填“金属”或“非金属”)元素,金属性比钙元素________(填“强”或“弱”),锶原子的核内质子数为________,原子核外有________个电子层,其原子结构示意图为________,其原子半径________镁(填“大于”、“小于”或“等于”);铯的原子核外共有________层电子,最外层电子数为________。
(2)铯与水起剧烈反应,放出________色气体,同时使滴有紫色石蕊试液的溶液显________色,因为______________________(写出化学方程式)。
(3)碳酸锶是________色粉末,与盐酸反应的离子方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机合成的重要中间体F的一种合成路线如下:
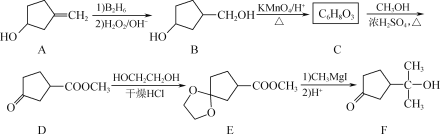
(1) F中含氧官能团的名称是________、________。
(2) C的结构简式为________。
(3) 从整个流程看,D→E的作用是___________。
(4) G为比E相对分子质量大14的同系物,H与G互为同分异构体且符合下列条件:
① 1 mol H能与2 mol NaHCO3反应;
② H能使溴的四氯化碳溶液褪色;
③ H分子中含有3种不同化学环境的氢。
则H的结构简式为________(写一种)。
(5) 写出以![]() 、CH3OH和CH3CH2MgI为主要原料制备
、CH3OH和CH3CH2MgI为主要原料制备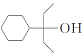 的合成路线____________ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线____________ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银由于其优良的性能和特性被广泛应用于照相、电子、电气等工业。废定影液中银主要以Na3Ag(S2O3)2形式存在,实验室用废定影液制备Ag的具体流程如图所示:
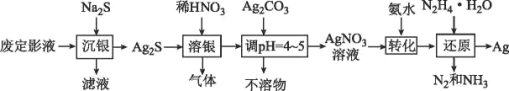
注意:“还原”时由于Ag+直接与N2H4H2O反应过于激烈,所以采用加入氨水,使Ag+与氨形成[Ag(NH3)2]+,降低Ag+的浓度,从而相应降低Ag+的氧化能力,使反应能够平稳进行。
回答下列问题:
(1)“溶银”时产生的气体是__(填物质的名称),得到1mol该气体转移电子为__mol。
(2)N2H4H2O(水合肼)为无色透明的油状发烟液体,具有强还原性,实验室制备原理为NaClO+2NH3=N2H4H2O+NaCl,可能用到的实验装置如图所示:
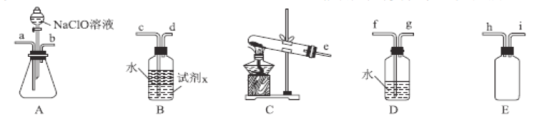
①本实验中用不到的装置是__(填字母),按气流从左到右的方向,整套装置的连接顺序为__(填仪器接口小写字母)。
②从氧化还原角度分析,上述反应中NaClO表现出的性质为__;加入NaClO溶液时要慢慢滴加,目的是__。
(3)AgNO3见光或受热易分解。将上述流程中AgNO3溶液蒸发浓缩可获得AgNO3固体,实验装置如图所示:

①使用真空泵的目的是__。
②测定AgNO3固体的纯度(杂质不参与反应)称取2.000g制备的AgNO3固体,加水溶解,定容到100mL;准确量取25.00mL溶液,酸化后滴入几滴NH4Fe(SO4)2溶液作指示剂,再用0.1000molL-1NH4SCN标准溶液滴定,消耗NH4SCN标准溶液的平均体积为29.00mL,则固体中AgNO3的质量分数为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现在含有生命元素硒(![]() )的保健品已经进入市场,已知硒与氧同族,与钾同周期,则下列关于硒的叙述中正确的是( )
)的保健品已经进入市场,已知硒与氧同族,与钾同周期,则下列关于硒的叙述中正确的是( )
A.硒单质在常温下是固体
B.硒的气态氢化物稳定性比![]() 强
强
C.硒是金属元素
D.硒酸(![]() )的酸性比硫酸强
)的酸性比硫酸强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生活密切相关。下列事实和解释均正确的是( )
选项 | 事实 | 解释 |
A | 单晶硅用于制造光导纤维 | 单晶硅可使光发生全反射 |
B | 泡沫灭火器是利用 |
|
C | 利用铝热剂( | 铝置换出铁吸收能量使铁凝固 |
D | 用乙醇洗去织物上的油污 | 乙醇能与油污发生取代反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象得出的结论正确的是( )
选项 | 操作 | 现象 | 结论 |
A | 将NaHCO3溶液滴入Ca(ClO)2溶液中 | 出现沉淀 | Ka2(H2CO3)> Ka (HClO) |
B | 将湿润的KI-淀粉试纸置于集满红棕色气体的集气瓶口 | 试纸变蓝 | 该气体为Br2 |
C | 将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液 | 出现沉淀 | 沉淀只有AgBr |
D | 将石蜡油蒸汽通过炽热的碎瓷片,再将生成的气体通入溴的CCl4溶液中 | 溶液褪色 | 石蜡油催化裂解生成不饱和烃 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入 6mol/L 的硫酸溶液,乙同学将电极放入 6mol/L 的氢氧化钠溶液中,如图所示:
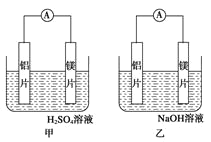
(1)写出甲电池中正极的电极反应式___________________ ;
(2)写出乙池中负极的电极反应式: 负极:_____ 总反应的离子方程式:_________
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金 属,则构成负极材料的金属活泼
,则甲会判断出_____活动性更强,而乙会判断出_____活动性更强(填名称)
(4)由此实验,可得到如下哪些正确结论(_____)
a. 利用原电池反应判断金属活动性顺序时应注意选择合适的介质
b. 镁的金属性不一定比铝的强
c. 该实验说明金属活动性顺序表已过时,已没有利用价值
d. 该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
(5)上述实验也反过来证明了“直接利用金属活动性顺序表判断原电池中的正负极”这种做法__填 “可靠”或“不可靠”)。如不可靠,请你提出另一个判断原电池正负极的可行实验方案_______________ (如 可靠,可不填)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置。
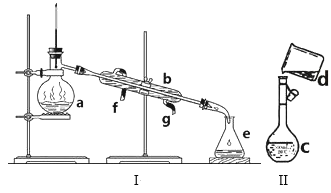
(1)写出下列仪器的名称:a.__ b.__ c.__。
(2)仪器a~e中,使用前必须检查是否漏水的有__。(填序号)
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是__,将仪器补充完整后进行实验,温度计水银球的位置在__处。冷凝水由__(填f或g)口通入,__口流出。
(4)现需配制0.1mol/LNaOH溶液500mL,装置II是某同学转移溶液的示意图。
①图中的错误是__。除了图中给出的的仪器和托盘天平外,为完成实验还需要的仪器有:___。
②根据计算得知,所需NaOH的质量为__g。
③配制时,正确操作顺序是(字母表示,每个字母只用一次)__。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
④用“偏大”“偏小”或“无影响”填空
A.配制NaOH溶液,需称量一定质量的溶质,称量时使用了游码,但物码放置颠倒__。
B.配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容__。
C.定容摇匀后,发现液面下降,继续加水至刻度线__。
D.定容时仰视刻度线__。
E.容量瓶中原有少量蒸馏水__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com