
【题目】25℃时,向某二元弱酸H2X的钠盐溶液中滴加盐酸,混合溶液中离子浓度与pH的关系如图所示,其中lgX = ![]() 或
或![]() 。下列叙述不正确的是
。下列叙述不正确的是

A. 曲线m表示![]() 与pH的变化关系
与pH的变化关系
B. Ka1(H2X)的数量级为10-7
C. 当溶液呈中性时, c(HX-)>c(X2-)>c(H2X)
D. 25℃时,NaHX溶液中:c(OH-)>c(H+)
【答案】C
【解析】
A. 因为H2X为二元弱酸,Ka1>>Ka2, 所以X2-的水解程度大,碱性强,故曲线m表示![]() 与pH的变化关系是正确的;B.当
与pH的变化关系是正确的;B.当![]() =1时,10c(H2X)= c(HX-),pH=7.4,c(H+)=10-7.4此时, Ka1(H2X)=c(H+)
=1时,10c(H2X)= c(HX-),pH=7.4,c(H+)=10-7.4此时, Ka1(H2X)=c(H+)![]() c(HX-)/c(H2X)=10-7.4
c(HX-)/c(H2X)=10-7.4 ![]() 10=10-6.4, Ka1(H2X)的数量级为10-7是正确的,故B正确;C.由图可知当溶液呈中性时,
10=10-6.4, Ka1(H2X)的数量级为10-7是正确的,故B正确;C.由图可知当溶液呈中性时,![]() <0, c(X2-)< c(HX-);当
<0, c(X2-)< c(HX-);当![]() >0
>0
c(HX-)> c(H2X),因为水解大于电离,所以(H2X)> c(X2-),故C错误; D.由图可知,当![]() =0即c(HX-)=c(HX-)时 ,pH>9.3,溶液显碱性,所以水解大于电离,NaHX溶液显碱性,c(OH-)>c(H+),故D正确;答案:C。
=0即c(HX-)=c(HX-)时 ,pH>9.3,溶液显碱性,所以水解大于电离,NaHX溶液显碱性,c(OH-)>c(H+),故D正确;答案:C。


科目:高中化学 来源: 题型:
【题目】在组成生物体的下列各组元素中,属于大量元素的一组是( )
A. C、H、O、Zn B. C、H、O、N C. N、P、S、Cu D. N、P、S、Mn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为了测定某品牌铝合金中铝的含量,现设计了如下实验:
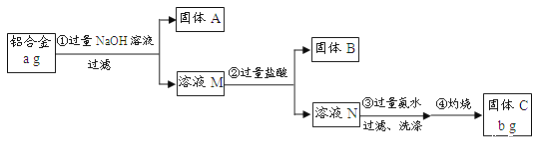
已知:该铝合金的主要成分为Al2O3、MgO、CuO、SiO2。
请回答下列问题:
(1)固体A的成分是_______;
(2)生成固体B的化学方程式为_____;步骤③中生成沉淀的离子方程式为_____;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为______;
(4)该样品中铝的质量分数是______;(用a、b表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列装置的叙述错误的是( )

A. X如果是硫酸铜,a和b分别连接直流电源正、负极,一段时间后铁片质量增加
B. X如果是氯化钠,则a和b连接时,该装置可模拟生铁在食盐水中被腐蚀的过程
C. X如果是硫酸铁,则不论a和b是否用导线连接,铁片均发生氧化反应
D. X如果是氢氧化钠,将碳电极改为铝电极,a和b用导线连接,此时构成原电池铁作负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质都是由分子构成,且都是共价化合物的一组是( )
A. 干冰、蔗糖水、液氧 B. 硫酸、液氨、酒精
C. 浓硫酸、氮气、葡萄糖 D. C60、 酒精、碳酸氢铵
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用A+、B-、C2-、D、E、F分别表示含有18个电子的几种微粒(离子或分子),请回答下列问题:
(1)A元素是________、B元素是________、C元素是_______(用元素符号表示)。
(2)B的单质可用来制“84”消毒液的主要成分,写出反应的离子方程式________________。
(3)用文字描述比较B、C两元素的非金属性强弱的方法(必要时可用方程式,至少一条):___________________________________。
(4)D是由两种元素组成的双原子分子,用电子式表示其形成过程________________。
(5)E是所有含18个电子的微粒中氧化能力最强的分子,其与水反应的化学方程式为___________________。
(6)F分子中含有4个原子,既有极性键又有非极性键,其电子式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物有如下转化关系:

(1)写出反应A→B的反应条件是____________,C中官能团的结构简式是______________。
(2)反应B→C的反应类型为____________。
(3) 在浓硫酸加热条件可以生成含有三个六元环结构的有机物,该有机物结构简式为:____________。
在浓硫酸加热条件可以生成含有三个六元环结构的有机物,该有机物结构简式为:____________。
(4)任意写出一种符合下列条件的C的同分异构体的结构简式______________
①属于芳香族化合物,苯环上有两个取代基
②与碳酸氢钠溶液反应放出二氧化碳气体
③苯环上的一氯代物有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)![]() 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
A. 2.5mol C B. 2 mol A、2 mol B和10 mol He(不参加反应)
C. 1.5 mol B和1.5 mol C D. 2 mol A、3 mol B和3 mol C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容中加入2.0molSO2和1.0molO2,一定条件下发生如下反应2SO2+O2![]() 2SO3。反应达到平衡后,各物质的物质的量可能为( )
2SO3。反应达到平衡后,各物质的物质的量可能为( )
n(SO2)/mol | n(O2)/mol | n(SO3)/mol | |
A | 2.0 | 1.0 | 0 |
B | 1.0 | 0.8 | 1.0 |
C | 0.20 | 0.10 | 1.80 |
D | 0 | 0 | 2.0 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com