
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):Cu+2H2SO4(浓) ![]() CuSO4+X↑+2H2O试通过计算和推理回答下面的问题:
CuSO4+X↑+2H2O试通过计算和推理回答下面的问题:
(1)X物质可以导致酸雨的形成,X应该属于________(填字母代号)。
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(2)X物质可以使酸性KMnO4溶液褪色,该过程中(填化学式,下同)______失去电子,氧化剂是______。
(3)足量的铜片与20mL18mol·L-1的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的物质的量为______mol,生成的X气体在标准状况下体积为______L(假设气体全部逸出)。
(4)将(3)反应后得到的溶液与过量Ba(OH)2溶液混合,充分反应,反应后所得沉淀的质量为______g。
【答案】d ![]()
![]() 0.1 2.24 70.38
0.1 2.24 70.38
【解析】
足量的铜片与20mL18mol·L-1的浓H2SO4混合,发生反应Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,虽然反应物与生成物中间用“==”,但由于稀硫酸与铜不反应,所以铜和硫酸都有剩余。在进行硫酸铜生成量的计算时,我们既不能利用铜,也不能利用硫酸进行计算。
CuSO4+SO2↑+2H2O,虽然反应物与生成物中间用“==”,但由于稀硫酸与铜不反应,所以铜和硫酸都有剩余。在进行硫酸铜生成量的计算时,我们既不能利用铜,也不能利用硫酸进行计算。
(1)对于Cu+2H2SO4(浓)![]() CuSO4+X↑+2H2O,利用质量守恒定律,可求出X的化学式为SO2,X应该属于酸性氧化物;
CuSO4+X↑+2H2O,利用质量守恒定律,可求出X的化学式为SO2,X应该属于酸性氧化物;
答案为:d;
(2)SO2可以使酸性KMnO4溶液褪色,则SO2作还原剂,该过程中SO2失去电子,氧化剂是KMnO4;
答案为:SO2;KMnO4;
(3)足量的铜片与20mL18mol·L-1的浓H2SO4充分反应,则存在下列关系式:Cu—2e-—H2SO4—CuSO4—SO2;该反应过程中转移了0.2mol电子,则n(CuSO4)=n(SO2)=![]() n(e-)=0.1mol,V(SO2)=0.1mol×22.4L/mol=2.24L;
n(e-)=0.1mol,V(SO2)=0.1mol×22.4L/mol=2.24L;
答案为:0.1;2.24;
(4)由上面计算可知,在铜与浓硫酸的反应中,n(Cu2+)=n(H2SO4)氧化性=0.1mol,从而得出溶液中n(SO42-)=0.020L×18mol/L-0.1mol=0.26mol;与过量Ba(OH)2溶液混合,发生如下反应:Cu2++2OH-=Cu(OH)2↓,Ba2++ SO42-= BaSO4↓,从而得出n[Cu(OH)2]=0.1mol,n(BaSO4)= 0.26mol,m(沉淀)=m[Cu(OH)2]+m(BaSO4)= 0.1mol×98g/mol+0.26mol×233g/mol=70.38g;
答案为:70.38。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】锌是人体必需的微量元素,在体内有着重要的功能,然而过度的Zn2+会引起毒性,因此能够高效、灵敏检测Zn2+的方法非常重要。化合物L对Zn2+有高识别能力和良好的抗干扰性,其合成路线可设计如下:
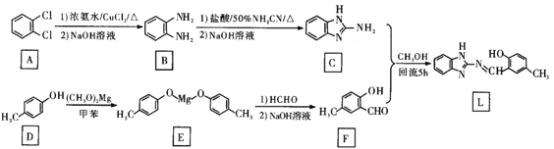
回答下列问题:
(1)A的化学名称为____________F的官能团名称为____________。
(2)D生成E的化学方程式为________________,该反应类型为____________。
(3)已知R-N=N-R分子中的N原子存在孤对电子(未共用电子对),且N = N双键不能旋转,因而存在顺反异构:![]() (顺式),
(顺式),![]() (反式)。判断化合物L是否存在顺反异构________(填“是”或“否”)。
(反式)。判断化合物L是否存在顺反异构________(填“是”或“否”)。
(4)研究人员利用某种仪器进行分析,发现化合物L中亚氨基(-NH-)及-OH上的氢原子的.吸收峰在结合Zn2+后的谱图中消失,该仪器的名称是___________仪;研究人员推测化合物L结合Zn2+的机理为:![]() 其中,Zn2+与-N=之间共价键的成键方式是________(填标号)。
其中,Zn2+与-N=之间共价键的成键方式是________(填标号)。
a. Zn2+和N原子各自提供单电子组成共用电子对
b. Zn2+单方面提供电子对与N原子共用
c. N原子单方面提供电子对与Zn2+共用
(5)X为F的芳香族同分异构体,写出满足如下条件的X的结构简式_____________。
①能发生水解反应和银镜反应,产物之一能与FeCl3溶液发生显色反应;
②有六种不同化学环境的氢,个数比为3:1:1:1:1:1。
(6)已知:通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。化合物Y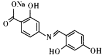 具有抑菌活性,以
具有抑菌活性,以![]() 和
和![]() 为原料制备Y,写出合成路线(有机溶剂和无机试剂任选)。____________。
为原料制备Y,写出合成路线(有机溶剂和无机试剂任选)。____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将红热的固体单质M放入浓硝酸中,剧烈反应,产生混合气体A,A在常温下不与空气接触时,发生如图所示的变化。

(1)混合气体A的主要成分是____________。
(2)气体B为__________,蓝色溶液D为____________。
(3)单质M与浓硝酸反应的化学方程式是____________________________。
(4)单质C与稀硝酸反应的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酸甲酯(CH2=CHCOOCH3)是一种重要的有机化工原料。实验室制备少量丙烯酸甲酯的反应为:CH2=CHCOOH+CH3OH![]() CH2=CHCOOCH3+H2O,步骤如下:
CH2=CHCOOCH3+H2O,步骤如下:
步骤1:在100mL圆底烧瓶中依次加入10.0g丙烯酸、少许碎瓷片、10mL甲醇和2mL浓硫酸,搅拌。
步骤2:如图,连接装置,加热烧瓶中的混合液,用锥形瓶盛接通过分水器分离出的水。当不再有水生成,停止加热。
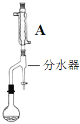
步骤3:反应液冷却后,依次用5%Na2CO3溶液、饱和食盐水、水洗涤。分离出有机相。
步骤4;向有机相中加无水Na2SO4固体,过滤后蒸馏,收集70~90℃馏分。测得丙烯酸甲酯的质量为6.45g。
可能用到的信息:
密度 | 沸点 | 溶解性 | ||
丙烯酸 | 1.05g·cm-3 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
甲醇 | 0.79g·cm-3 | 65℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
丙烯酸甲酯 | 0.95g·cm-3 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
请回答下列问题:
(1)步骤1中,加入碎瓷片的目的是__。
(2)步骤2中,图中所示装置中仪器A的名称是__,其作用为__。
(3)步骤3中,用5%Na2CO3溶液洗涤后,分离有机相的操作名称为__。
(4)实验中可能生成的有机副产物结构简式为__(填一种即可)。
(5)本实验中丙烯酸甲酯的产率为__%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香草醛又名香兰素,是食品和药品的重要原料,其结构简式如图所示。下列有关香草醛的说法中不正确的是( )

A.香草醛可以发生银镜反应
B.在一定条件下1mol香草醛可以与4molH2反应
C.香草醛遇FeCl3溶液可变色
D.香草醛可与NaOH溶液反应,也可与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是
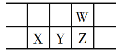
A. 原子半径:W<X
B. 常温常压下,Y单质为固态
C. 气态氢化物热稳定性:Z<W
D. X的最高价氧化物的水化物是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热蒸干氯化镁溶液时因水解不完全会得到一种灰白色沉淀——碱式氯化镁,化学式可表示为Mgx(OH)yClz·nH2O,设计如图装置验证其化学式。下列有关实验的说法不正确的是( )
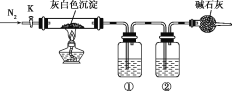
A.碱式氯化镁受热分解可以生成氧化镁、氯气和水
B.结束反应时,先停止加热,通一段时间N2后再关闭活塞K
C.①②中依次盛装浓硫酸、氢氧化钠溶液
D.只需称量原样品质量、反应结束后硬质玻璃管中剩余固体质量以及装置①增重的质量即可推出其化学式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,a、b是两根石墨棒。下列叙述正确的是( )
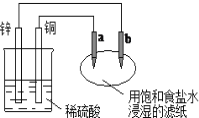
A.a是正极,发生还原反应
B.b是阳极,发生氧化反应
C.往滤纸上滴加酚酞试液,a极附近颜色变红
D.稀硫酸中硫酸根离子的物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海底蕴藏着丰富的锰结核矿,其主要成分是MnO2。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的MnO2,其工艺流程如图所示:
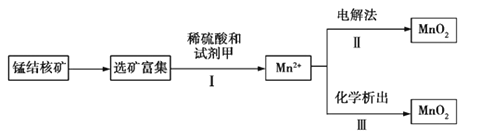
已知:化学析出时用NaClO3作析出试剂,每生成0.05 mol MnO2时消耗0.02 mol NaClO3。
根据以上工艺流程及信息,判断下列说法不正确的是
A.步骤Ⅰ中的试剂甲必须具有较强的还原性
B.步骤Ⅲ发生反应的离子方程式为2ClO3—+5Mn2++4H2O=5MnO2+Cl2+8H+
C.若用电解法,则MnO2将在阳极产生,电极反应式为Mn2+-2e-+2H2O=MnO2+4H+
D.测定步骤Ⅰ所得溶液中Mn2+的含量可采用先将Mn2+转化为Mn,然后再用0.1 mol·L-1 HCl标准溶液滴定的方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com