
【题目】氯苯是燃料、医药、有机合成的中间体,是重要的有机化工产品。实验室制取氯苯的装置如图所示(加热和固定仪器的装置略去)。回答下列问题:
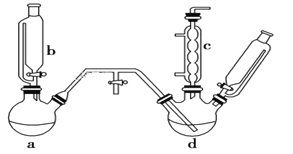
(1)a和b仪器组合成制取氯气的装置,反应无需加热,则a装置中的固体反应物可以是________(填字母序号)。
A.MnO2 B.KMnO4 C.K2Cr2O7
(2)把氯气通入反应器d中(d装置有FeCl3和苯),加热维持反应温度40~60 ℃,温度过高会生成过多的二氯苯。对d加热的方法是______________________。
(3)装置c出口的气体成分有HCl、Cl2、水蒸气和_____。
(4)制取氯苯的化学方程式为_______________________ 。
(5)装置d中的反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏。
①碱洗之前要水洗,其目的是______________________________。
②用10%NaOH溶液碱洗时发生氧化还原反应的化学反应方程式为_____________________。
(6)生成的氯气中存在HCl、H2O等杂质气体,若需要增加一个装置除去水蒸气,请画出该装置图,并标明所用试剂________。
(7)工业生产中苯的流失情况如下表所示:
项目 | 二氯苯 | 氯化尾气 | 蒸气 | 成品 | 不确定苯耗 | 合计 |
苯流失量kg/t | 11.7 | 5.4 | 20.8 | 2.0 | 49.3 | 89.2 |
则10t苯可制得成品氯苯________t(列出计算式即可。氯苯和苯的相对分子质量分别是112.5和78)。
【答案】 BC 水浴加热 苯蒸气 ![]() 洗去FeCl3、Cl2、HCl等无机物,节省碱的用量,降低成本 Cl2+2NaOH===NaCl+NaClO+H2O
洗去FeCl3、Cl2、HCl等无机物,节省碱的用量,降低成本 Cl2+2NaOH===NaCl+NaClO+H2O 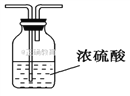 10×(1-0.089 2)×
10×(1-0.089 2)×![]()
【解析】(1)高锰酸钾和重铬酸钾氧化性强,二氧化锰制氯气需要加热,高锰酸钾和重铬酸钾不用,
故选BC;(2)反应器C加热控制反应温度在40-60℃,可利用水浴加热;(3)仪器c为球形冷凝管,由于苯易挥发,反应产生的HCl,且有未反应的氯气,D出口气体中含有HCl、苯蒸汽、氯气;(4)制取氯苯的化学方程式为![]() ;(5)①d中反应完成后有l3、HCl等副产品,易溶于水,碱洗之前要水洗,可以洗去这些无机物,节约碱的用量,降低成本;②催化剂氯化铁与氢氧化钠反应,生成HCl会与氢氧化钠反应,溶解的氯气也会与氢氧化钠反应,该反应为氧化还原反应:Cl2+2NaOH=NaCl+NaClO+H2O;(6)浓硫酸用于吸收水蒸气,导气管应长进短出,装置为:
;(5)①d中反应完成后有l3、HCl等副产品,易溶于水,碱洗之前要水洗,可以洗去这些无机物,节约碱的用量,降低成本;②催化剂氯化铁与氢氧化钠反应,生成HCl会与氢氧化钠反应,溶解的氯气也会与氢氧化钠反应,该反应为氧化还原反应:Cl2+2NaOH=NaCl+NaClO+H2O;(6)浓硫酸用于吸收水蒸气,导气管应长进短出,装置为: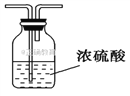 ;(7)苯的总流失量为89.2Kg/t,故1t苯中参加反应的苯的质量为(1t-0.0892t),由苯与氯苯质量之比为78:112.5,则10t 苯可制得成品氯苯为:10×(1-0.089 2)×
;(7)苯的总流失量为89.2Kg/t,故1t苯中参加反应的苯的质量为(1t-0.0892t),由苯与氯苯质量之比为78:112.5,则10t 苯可制得成品氯苯为:10×(1-0.089 2)×![]() t;
t;


科目:高中化学 来源: 题型:
【题目】有关如下所示化合物的说法不正确的是( )

A. 既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B. 1mol该化合物最多可以与3molNaOH反应
C. 既可以催化加氢,又可以使酸性KMnO4溶液褪色
D. 既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用氯酸钾和二氧化锰制取氧气的反应方程式为:2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
回答下列问题:
(1)该反应中被氧化的元素名称为______,生成1mol![]() 时转移电子的数目是______。
时转移电子的数目是______。
(2)从反应后的固体混合物中分离出难溶于水的![]() 的具体实验操作步骤:______。
的具体实验操作步骤:______。
(3)分离出的![]() 可用于实验室制取
可用于实验室制取![]() ,化学方程式为:MnO2+4HCl(浓)
,化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,其离子方程式为____。
MnCl2+Cl2↑+2H2O,其离子方程式为____。
(4)若两个反应中转移的电子的物质的量相同,则生成的![]() 和
和![]() 在相同状况下的体积比为____。
在相同状况下的体积比为____。
(5)以上两个反应都用到![]() ,其作用分别是 ______、_________。
,其作用分别是 ______、_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,如下图为两套实验装置。

(1)写出下列仪器的名称:①______________ ④_______________。
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器是___________,冷凝管的进水口是_________(填“f”或“g”)。
(3)某校环保兴趣小组在处理污水样品时,需用质量分数为36.5% 、密度为1.2g/cm3 的浓盐酸配制成250mL 0.1mol/L的稀盐酸溶液。装置Ⅱ是某同学转移溶液的示意图,图Ⅱ中的两处错误分别是______。
(4)根据计算,本实验需要量取浓盐酸的体积为_______ mL,本实验应使用的量筒是___。(在横线上填写相应的字母,否则无分,下同)
10mLB. 50mLC. 100mLD. 250mL
(5)在容量瓶的使用方法中,下列操作正确的是____________________。
A. 使用容量瓶前检查它是否漏水
B. 容量瓶用水洗净后,再用配好的稀HCl溶液润洗
C. 配制溶液时,如果试样是固体,把称好的试样用纸槽小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
D. 配制溶液时,若试样是液体,用量筒取试样后直接倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
E. 盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在容积不变的密闭容器中注满NO2气体,2NO2(g)N2O4(g)△H<0.平衡后把该容器置于沸水中,下列性质或数值不会改变的是( )
①颜色 ②平均摩尔质量 ③质量 ④压强 ⑤密度.
A.①② B.②③ C.④⑤ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将潮湿的Cl2通过甲装置后,再通过放有干燥红色布条的 乙装置,红色布条不褪色,则甲装置中所盛试剂可能是

①浓硫酸 ②饱和食盐水 ③水 ④NaOH溶液
A. ①② B. ②③ C. ①④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.100molL-1的盐酸滴定10ml0.100molL-1的Na2CO3溶液.溶液pH值与加入盐酸的体积的关系如图所示,已知室温时饱和CO2的pH为3.9,0.05molL-1NaHCO3的pH约为8.3,下列说法不正确的是
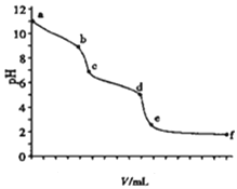
A. 以酚酞为指示剂,溶液颜色发生突变时(b点),Na2CO3转化为NaHCO3
B. 以甲基橙为指示剂,溶液颜色发生突变时,共消耗盐酸20.00ml
C. 溶液pH=7(c点),碳酸钠完全转化为NaCl
D. ce段对应溶液中CO2与NaHCO3共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实。2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) 下列叙述错误的是
CH3CH2OH(g)+3H2O(g) 下列叙述错误的是
A. 使用Cu-Zn-Fe催化剂可大大提高生产效率
B. 反应需在300℃进行可推测该反应是吸热反应
C. 充入大量CO2气体可提高H2的转化率
D. 从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com