
| A、CaCl2溶液 |
| B、NaAlO2溶液 |
| C、Na2CO3溶液 |
| D、水玻璃 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、充入的CO分子数比CO2分子数少 |
| B、甲容器的体积比乙容器的体积小 |
| C、CO的摩尔体积比CO2的摩尔体积小 |
| D、甲中CO的密度比乙中CO2的密度小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe与FeCl3溶液反应:Fe+Fe3+=2Fe2+ |
| B、往AlCl3溶液中滴入氨水:Al3++3OH-=Al(OH)3↓ |
| C、铁与稀盐酸反应:Fe+2H+=Fe2++H2↑ |
| D、氯化钡与硫酸反应:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 乙酸 | 1-丁醇 | 乙酸丁酯 | |
| 熔点/℃ | 16.6 | -89.5 | -73.5 |
| 沸点/℃ | 117.9 | 117 | 126.3 |
| 密度/g?cm-3 | 1.05 | 0.81 | 0.88 |
| 水溶性 | 互溶 | 互溶 | 不溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室用如图装置制取乙酸乙酯.
实验室用如图装置制取乙酸乙酯.查看答案和解析>>
科目:高中化学 来源: 题型:
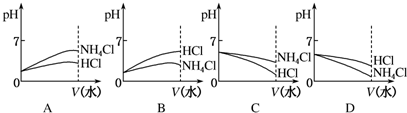
查看答案和解析>>
科目:高中化学 来源: 题型:
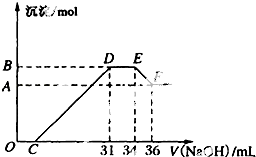 某同学取一定量的Al、Fe混合物,与2.0L极稀的HNO3充分反应,假设HNO3的还原产物全部为铵盐.在反应后的溶液中,逐滴加入4mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示.分析图象回答问题:
某同学取一定量的Al、Fe混合物,与2.0L极稀的HNO3充分反应,假设HNO3的还原产物全部为铵盐.在反应后的溶液中,逐滴加入4mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示.分析图象回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com