
标准状况下,用一定量的水吸收氨气气制得浓度为12.0mol/L、密度为0.915g/cm3的氨水。试计算1体积的水吸收多少体积的氨气可制得上述氨水。
科目:高中化学 来源: 题型:
铜的冶炼过程大致可分为:①富集,将硫化物矿进行浮选 ②焙烧,主要反应为:2CuFeS2+4O2===Cu2S+3SO2+2FeO(炉渣) ③制粗铜,在1 200 ℃主要反应为:2Cu2S+3O2===2Cu2O+2SO2;2Cu2O+Cu2S===6Cu+SO2↑ ④电解精炼铜
下列说法不正确的是
A.冶炼过程中的尾气可用来制硫酸
B.上述过程中,由1 mol CuFeS2制取1 mol Cu时共消耗2 mol O2
C.在反应2Cu2O+Cu2S===6Cu+SO2↑中,氧化剂是Cu2O和Cu2S
D.电解精炼铜的过程中,每转移1 mol电子时,阳极溶解铜的质量小于32 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.有机物种类繁多的主要原因是有机物分子结构十分复杂
B.烃类分子中的碳原子与氢原子是通过极性键结合的
C.同分异构现象的广泛存在是造成有机物种类繁多的唯一原因
D.烷烃的结构特点是碳原子通过单键连接成链状,剩余价键均与氢原子结合
查看答案和解析>>
科目:高中化学 来源: 题型:
硫磺在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,乙溶液褪色变成丙。在丙里加入Na2S生成气体丁,把丁通入乙得到沉淀戊。甲、乙、丙、丁、戊均含有硫元素,则它们正确的顺序是( )
A.SO3 H2SO4 H2SO3 H2S S B.SO2 H2SO3 H2SO4 SO2 SO3
C.SO3 H2SO4 H2SO3 SO2 Na2S2O3 D.SO2 H2SO3 H2SO4 H2S S
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上硝酸的制备和自然界中硝酸的生成既有相同之处,又有区别。路线①②③是工业生产硝酸的主要途径,路线Ⅰ、Ⅱ、Ⅲ是雷电高能固氮过程中硝酸的生成途径。
|
|
|
|
|
 N2 → NH 3 → NO → NO2 → HNO3
N2 → NH 3 → NO → NO2 → HNO3
|
(1)写出工业制硝酸各步反应化学方程式
。
(2)硝酸生产排放出的NO是污染物,有一治理法,是在4000C且有催化剂作用下,用氨把NO还原成无色无味气体,其化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从小到大的是
A.p (Ne) < p (H2) < p (O2) B.p (O2) < p (Ne) < p (H2)
C.p (H2) < p (O2) < p (Ne) D.p (H2) < p (Ne) < p (O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是四种常见有机物的比例模型示意图。下列说法正确的是
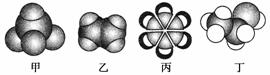
A.甲能使酸性KMnO4溶液褪色
B.乙可与溴水发生取代反应而使溴水褪色
C.丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特键
D.丁在稀硫酸作用下可与乙酸发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
 淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去):实验过程如下:①将1∶1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30 min,然后逐渐将温度降至60℃左右;②将一定量的淀粉水解液加入三颈烧瓶中;③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3、98%H2SO4的质量比为2:1.5)溶液;④反应3h左右,冷却,过滤后再重结晶得草酸晶体。
淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去):实验过程如下:①将1∶1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30 min,然后逐渐将温度降至60℃左右;②将一定量的淀粉水解液加入三颈烧瓶中;③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3、98%H2SO4的质量比为2:1.5)溶液;④反应3h左右,冷却,过滤后再重结晶得草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O 3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的目的是: ▲ 。
(2)冷凝水从a口进入,但实验中若混酸滴加过快,将导致草酸产量下降,其原因是 ▲ 。
(3)检验淀粉是否水解完全所用的试剂为 ▲ 。
(4) 当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NOx全部吸收,发生的化学反应方程式为: ▲ 。
 (5) 将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸。用KMnO4标准溶液滴定,该反应的离子方程式为:2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ + 10CO2↑+ 8H2O
(5) 将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸。用KMnO4标准溶液滴定,该反应的离子方程式为:2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ + 10CO2↑+ 8H2O
称取该样品0.12 g,加适量水完全溶解,然后用0.020 mol·L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),此时滴定终点的现象为 ▲ 。滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示装置进行实验(夹持装置已略去)。请回答下列问题:
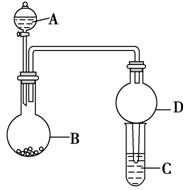
(1)若A中为浓硫酸,B中为铁单质,C中为氢氧化钠溶液。将浓硫酸滴入B中,则B中将发生________现象;铁元素在周期表中的位置为____________________;基态铁原子核外电子排布式为________________________________________________________________________。
(2)若A中为浓硝酸,B中为铜单质,C中为氢氧化钠溶液。将浓硝酸滴入B中,则B中发生反应的化学方程式为_______________________________________________。
(3)若A中为浓氨水,B中为某固体,C中为明矾溶液。
①将浓氨水逐滴滴入B中,可产生大量氨气,则B中固体可能是________(填序号)。
a.CaO b.NaOH
c.NaCl d.P2O5
②C中通入过量氨气时,反应的离子方程式为________________________________。
(4)若A中为稀盐酸,B中为碳酸钙,C中为NaAlO2溶液,将稀盐酸滴入B中后,B中反应的离子方程式为_____________________________________________________________;
不考虑HCl的挥发,若产生的气体足量,则C中发生反应的离子方程式为________________________________________________________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com