
美、德两国成功合成具有化学特性的氢铝化合物(AlH3)n,关于氢铝化合物的推测不正确的是 ( )。
A.氢铝化合物与水反应生成氢氧化铝和氢气
B.氢铝化合物中铝显+3价,氢显-1价
C.铝与水蒸气在高温下反应可生成氢铝化合物
D.氢铝化合物具有强还原性
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014年高考化学苏教版总复习 1-4 氧化还原反应练习卷(解析版) 题型:选择题
根据反应:2H2S+O2=2S↓+2H2O,Na2S+I2=2NaI+S↓,4NaI+O2+2H2SO4=2I2+2Na2SO4+2H2O,下列物质的氧化性强弱判断正确的是( )
A.O2>I2>S B.H2S>NaI>H2O
C.S>I2>O2 D.H2O>NaI>H2S
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-1 物质的分类、转化及分散系练习卷(解析版) 题型:选择题
下列有关溶液和胶体的叙述正确的是 ( )
A.Fe(OH)3胶体和FeCl3溶液区别的本质特征为是否具有丁达尔效应
B.FeCl3溶液呈电中性,Fe(OH)3胶体带有电荷
C.纳米材料的微粒直径从几纳米到几十纳米,因此纳米材料是胶体
D.FeCl3溶液能使血液凝聚沉降
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-3铁、铜的获取及应用练习卷(解析版) 题型:选择题
向某晶体的溶液中加入含Fe2+的溶液无明显变化,当滴加几滴溴水后,混合液出现红色,由此得出下列的结论错误的是 ( )。
A.Fe3+的氧化性比溴的氧化性强
B.该晶体中一定含有SCN-
C.Fe2+与SCN-不能形成红色化合物
D.Fe2+被溴氧化成Fe3+
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-2从铝土矿到铝合金练习卷(解析版) 题型:选择题
将铝粉与Fe3O4粉末配制成铝热剂,分成三等份。
①一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为V1;
②一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为V2;
③一份直接放入足量的盐酸中,充分反应后放出气体在标准状况下的体积为V3。
下列说法正确的是 ( )。
A.V1=V3>V2 B.V2>V1=V3
C.V1=V2>V3 D.V1>V3>V2
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-1钠、镁及其化合物练习卷(解析版) 题型:选择题
现有25 mL 2 mol·L-1 Na2CO3和75 mL 1 mol·L-1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中;②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况是( )。
A.均为0.84 L B.均为0.56 L
C.①>② D.②>①
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习2-3-1氧化还原反应概念和规律练习卷(解析版) 题型:填空题
L、M、R、P、Q分别代表五种含不同化合价的氮元素的物质。A、B分别代表两种含不同化合价的氯元素的物质(每种物质中氮或氯元素的化合价只有一种)。又知物质M中的氮元素化合价要比物质Q中氮元素的化合价低。在一定条件下,它们会发生如下的转化(关系式未配平):
①P+A―→Q+B ②L+O2―→M+H2O ③L+M―→R+H2O ④B+H2O―→A+O2
(1)若五种含氮元素的物质中,有一种是硝酸,则硝酸是 ,理由是 。
(2)反应②必须在催化剂(铂、氧化铁等)作用下,加热到一定温度时方能发生,此反应在化工生产上有重要用途,据此推断在同温同压下,若物质R密度比空气的密度小,则R的化学式为 。
(3)某同学写出下面三个含氮的物质相互转换的关系式:
Ⅰ.M+P―→N2O3+H2O
Ⅱ.N2O4+H2O―→P+Q
Ⅲ.M+L―→Q+H2O
其中一定不可能实现的是 ,理由是 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习2-2电解质 离子反应练习卷(解析版) 题型:选择题
下列实验现象所对应的离子方程式不正确的是 ( )。
选项实验现象离子方程式
A将稀硫酸滴加到KI淀粉溶液中在空气中放置一段时间后溶液呈蓝色4H++4I-+O2=2I2+2H2O
B用硫氰化钾溶液检验某溶液中含有Fe3+溶液变成红色Fe3++3SCN-= Fe(SCN)3
C酸性KMnO4溶液中加入Na2SO3溶液溶液紫色褪去2MnO4-+5SO32-+6H+ =2Mn2++5SO42-+3H2O
D将稀硫酸滴加到含有酚酞的Ba(OH)2溶液中有白色沉淀生成,溶液由红色变成无色Ba2++OH-+H++SO42- =BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习1-1-2物质的分离和提纯练习卷(解析版) 题型:填空题
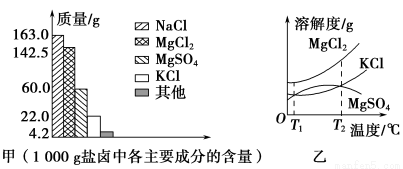
我国拥有很长的海岸线,具有丰富的海洋资源,以海水为原料的盐化工是我国重要的产业。盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如下图甲)。盐卤在食品、化工等方面具有广泛的用途。请解答下列与盐卤有关的试题。
(1)根据图甲,写出盐卤中含量最多的两种盐的化学式: 、 。
(2)下图乙是盐卤中某些物质的溶解度曲线,已知T1 ℃时,MgSO4和KCl的溶解度分别为M、N,则它们溶解度大小的关系为 ;将盐卤加热到T2 ℃以上,根据溶解度曲线,首先从盐卤中分离出来的晶体是 。
(3)化工厂利用卤水生产金属镁的工艺流程如下:
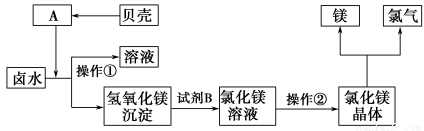
“操作①”的目的是将氢氧化镁沉淀分离出来,操作①的名称是 。氢氧化镁与试剂B反应的化学方程式为 。
操作②的名称是 。该方法的优点为 。
(4)用电解法制备金属镁,两位同学分别设计了下面的两种方法。
甲:电解氯化镁溶液。
乙:电解熔融的氯化镁。
其中同学 (填“甲”或“乙”)能够成功地制备金属镁,假设生产过程中镁元素没有损失,则100 g卤水可制备镁 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com