
| A£® | Ėį | B£® | ¼ī | C£® | ŃĪ | D£® | Ńõ»ÆĪļ |
·ÖĪö µēĄėŹ±Éś³ÉµÄŃōĄė×ÓČ«²æŹĒH+µÄ»ÆŗĻĪļĪŖĖį£»
µēĄėŹ±Éś³ÉµÄŅõĄė×ÓČ«²æŹĒOH-µÄ»ÆŗĻĪļĪŖ¼ī£»
½šŹōĄė×Ó»ņļ§øłĄė×Ó£ØNH4+£©ÓėĖįøłĄė×Ó»ņ·Ē½šŹōĄė×Ó½įŗĻµÄ»ÆŗĻĪļĪŖŃĪ£»
Ęä¹¹³ÉÖŠÖ»ŗ¬Į½ÖÖŌŖĖŲ£¬ĘäÖŠŅ»ÖÖŅ»¶ØĪŖŃõŌŖĖŲ£¬ĮķŅ»ÖÖČōĪŖ½šŹōŌŖĖŲ£¬ŌņĪŖ½šŹōŃõ»ÆĪļ£»ČōĪŖ·Ē½šŹō£¬ŌņĪŖ·Ē½šŹōŃõ»ÆĪļ£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗÉśŹÆ»Ņ»ÆѧŹ½ĪŖ£ŗCaO£¬ÓŠO”¢CaĮ½ÖÖŌŖĖŲ£¬ŹōÓŚŃõ»ÆĪļ£¬
¹ŹŃ”£ŗD£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪļÖŹµÄ·ÖĄą£¬ŹģĻ¤Ėį”¢¼ī”¢ŃĪ”¢Ńõ»ÆĪļøÅÄīŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®


 æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø
æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø ĆūĢāѵĮ·ĻµĮŠ“š°ø
ĆūĢāѵĮ·ĻµĮŠ“š°ø ĘŚÄ©¼Æ½įŗÅĻµĮŠ“š°ø
ĘŚÄ©¼Æ½įŗÅĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
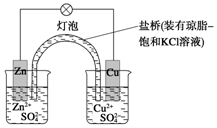 ĶŠæŌµē³Ų£ØČēĶ¼£©¹¤×÷Ź±
ĶŠæŌµē³Ų£ØČēĶ¼£©¹¤×÷Ź±²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 Ņ»¶ØĢõ¼žĻĀ£¬Ģå»żĪŖ10LµÄĆܱÕČŻĘ÷ÖŠ£¬1molXŗĶ1mol Y½ųŠŠ·“Ó¦£ŗ2X£Øg£©+2Y£Øg£©?Z£Øg£©£¬¾60s“ļµ½Ę½ŗā£¬Éś³É0.3molZ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
Ņ»¶ØĢõ¼žĻĀ£¬Ģå»żĪŖ10LµÄĆܱÕČŻĘ÷ÖŠ£¬1molXŗĶ1mol Y½ųŠŠ·“Ó¦£ŗ2X£Øg£©+2Y£Øg£©?Z£Øg£©£¬¾60s“ļµ½Ę½ŗā£¬Éś³É0.3molZ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ČōÉżøßĪĀ¶Č£¬XµÄĢå»ż·ÖŹżŌö“ó£¬ŌņÕż·“Ó¦µÄ”÷H£¾0 | |
| B£® | ½«ČŻĘ÷Ģå»ż±äĪŖ20L£¬ZµÄĘ½ŗāÅØ¶Č±äĪŖŌĄ“µÄ$\frac{1}{2}$ | |
| C£® | ŅŌXÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ0.001mol/£ØL•s£© | |
| D£® | ČōĶ¼×Ż×ų±źŹĒÕż·“Ó¦ĖŁĀŹ£¬Ōņ·“Ó¦Ó¦øĆŌŚ¾ųČČĢõ¼žĻĀ½ųŠŠ£¬Ķ¼Ļó×īøßµćĪŖĘ½ŗāµć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £Ø1£©8.4g N2Óė9.6gijµ„ÖŹRxĖłŗ¬Ō×ÓøöŹżĻąĶ¬£¬ĒŅ·Ö×ÓŹżÖ®±ČĪŖ3£ŗ2£¬ŌņRµÄĻą¶ŌŌ×ÓÖŹĮæŹĒ16£¬xÖµĪŖ3£®
£Ø1£©8.4g N2Óė9.6gijµ„ÖŹRxĖłŗ¬Ō×ÓøöŹżĻąĶ¬£¬ĒŅ·Ö×ÓŹżÖ®±ČĪŖ3£ŗ2£¬ŌņRµÄĻą¶ŌŌ×ÓÖŹĮæŹĒ16£¬xÖµĪŖ3£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĶ¬Ņ»øöµĪ¹ÜČ”ÓĆ²»Ķ¬µÄŅ©Ę· | |
| B£® | ½«ŹµŃéÖŠŹ£ÓąµÄŅ©Ę··Å»ŲŌŹŌ¼ĮĘæ | |
| C£® | ŹµŃéĒ°¶ŌŹµŃé×°ÖĆ½ųŠŠĘųĆÜŠŌ¼ģ²é | |
| D£® | ½«ŹµŃéŹŅÖʱøµÄæÉČ¼ŠŌĘųĢåÖ±½ÓµćČ¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 122.5 g KClO 3ÖŠŗ¬Cl-ŹżÄæĪŖNA | |
| B£® | 1 mol/LµÄNaOHČÜŅŗÖŠŗ¬Na+ŹżÄæĪŖNA | |
| C£® | ±ź×¼×“æöĻĀ£¬22.4 LĖ®ÖŠŗ¬ĒāŌ×ÓŹżÄæĪŖ2NA | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬32 g S03ÖŠŗ¬ŃõŌ×ÓŹżÄæĪŖ1.2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 µÄĆū³Ę2-Ļõ»ł¼×±½£ØĮŚĻõ»ł¼×±½£©£®
µÄĆū³Ę2-Ļõ»ł¼×±½£ØĮŚĻõ»ł¼×±½£©£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com