
ijČÜŅŗÖŠ“óĮæ“ęŌŚČēĻĀĪåÖÖĄė×Ó£ŗNO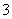 ”¢SO
”¢SO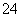 ”¢Fe3£«”¢H£«”¢M£¬ĖüĆĒµÄĪļÖŹµÄĮæÖ®±ČŅĄ“ĪĪŖn(NO
”¢Fe3£«”¢H£«”¢M£¬ĖüĆĒµÄĪļÖŹµÄĮæÖ®±ČŅĄ“ĪĪŖn(NO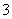 )”Ćn(SO
)”Ćn(SO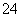 )”Ćn(Fe3£«)”Ćn(H£«)”Ćn(M)£½2”Ć3”Ć1”Ć3”Ć1£¬ŌņMæÉÄÜŹĒ£ŗ
)”Ćn(Fe3£«)”Ćn(H£«)”Ćn(M)£½2”Ć3”Ć1”Ć3”Ć1£¬ŌņMæÉÄÜŹĒ£ŗ
A£®Al3£«”””” B£®Mg2£« C£®CO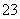 ”””” D£®Ba2£«
”””” D£®Ba2£«
 æŚĖćĢāæؼÓÓ¦ÓĆĢā¼ÆѵĻµĮŠ“š°ø
æŚĖćĢāæؼÓÓ¦ÓĆĢā¼ÆѵĻµĮŠ“š°ø ×ŪŗĻ×Ō²āĻµĮŠ“š°ø
×ŪŗĻ×Ō²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ę»¹ūĖįµÄ½į¹¹¼ņŹ½ĪŖ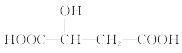 £¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
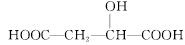 A£® ÓėĘ»¹ūĖį»„ĪŖĶ¬·ÖŅģ¹¹Ģå
A£® ÓėĘ»¹ūĖį»„ĪŖĶ¬·ÖŅģ¹¹Ģå
B£®1 molĘ»¹ūĖįæÉÓė3 mol NaOH·¢ÉśÖŠŗĶ·“Ó¦
C£®1 molĘ»¹ūĖįÓė×ćĮ潚ŹōNa·“Ӧɜ³É1 mol H2
D£® ĖÄĮŖ±½µÄŅ»ĀČ“śĪļÓŠ5ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŹµŃé×°ÖĆÉč¼ĘÕżČ·”¢ĒŅÄÜ“ļµ½ÄæµÄµÄŹĒ £Ø £©
|
|
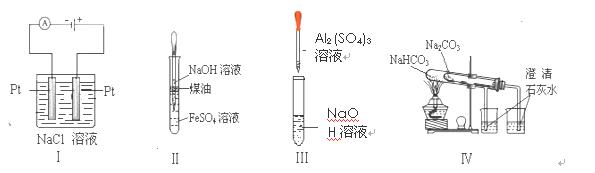
A£®ŹµŃé¢ń£ŗÖʱø½šŹōÄĘ B£®ŹµŃé¢ņ£ŗÖĘČ”ĒāŃõ»ÆŃĒĢś²¢¹Ū²ģĘäŃÕÉ«
C£®ŹµŃé¢ó£ŗÖĘȔɣĮæµÄĒāŃõ»ÆĀĮ D£®ŹµŃé¢ō£ŗ±Č½ĻĮ½ÖÖĪļÖŹµÄČČĪČ¶ØŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĮŖŗĻ¹śĘųŗņ±ä»Æ“ó»į2009Äź12ŌĀ7ČÕŌŚµ¤ĀóŹ×¶¼øē±¾¹žøłĄæŖį”Ä»£¬½µµĶ“óĘųÖŠCO2µÄŗ¬Įæ¼°ÓŠŠ§µŲæŖ·¢ĄūÓĆCO2£¬ŅżĘšĮĖø÷¹śµÄĘÕ±éÖŲŹÓ”£
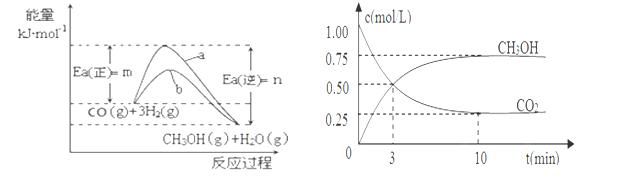
¹¤ŅµÉĻÓŠŅ»ÖÖ·½·ØŹĒÓĆCO2Ą“Éś²śČ¼ĮĻ¼×“¼£¬298.15KŹ±£¬CO2”¢H2”¢ÓėCH3OH”¢H2OµÄĘ½¾łÄÜĮæÓėŗĻ³É¼×“¼·“Ó¦µÄ»ī»ÆÄܵÄĒśĻßĶ¼ČēĶ¼1ĖłŹ¾£¬¾ŻĶ¼»Ų“šĪŹĢā£ŗ
£Ø1£©Š“³öŗĻ³É¼×“¼·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ £»
 Ķ¼1 Ķ¼2
Ķ¼1 Ķ¼2
£Ø2£©ŌŚĶ¼ÖŠĒśĻß £ØĢī”°a”±»ņ”°b”±£©±ķŹ¾¼ÓČė“߻ƼĮµÄÄÜĮæ±ä»ÆĒśĻß”£
£Ø3£©ŌŚĢå»żĪŖl LµÄĆܱÕČŻĘ÷ÖŠ£¬³äČėlmolCO2ŗĶ3molH2£¬²āµĆCO2ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼2ĖłŹ¾£®
¢Ł“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹv(H2)£½___________mol/(L”¤min)”£
¢ŚøĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ__________________£¬ÉżøßĪĀ¶Č£¬KÖµ £ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
¢ŪĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹n(CH3OH)£Æn(CO2)Ōö“óµÄŹĒ___________”£
A£®ÉżøßĪĀ¶Č B£®³äČėHe(g)£¬Ź¹ĢåĻµŃ¹ĒæŌö“ó
C£®½«H2O(g)“ÓĢåĻµÖŠ·ÖĄė D£®ŌŁ³äČė1mol CO2ŗĶ3mol H2
£Ø4£©ŌŚŌŲČĖŗ½ĢģĘ÷µÄÉśĢ¬ĻµĶ³ÖŠ£¬²»½öŅŖĒó·ÖĄėČ„³żCO2£¬»¹ŅŖĒóĢį¹©³ä×ćµÄO2”£Ä³ÖÖµē»ÆѧװÖĆæÉŹµĻÖČēĻĀ×Ŗ»Æ£ŗ2CO2£½2CO£«O2£¬COæÉÓĆ×÷Č¼ĮĻ”£ŅŃÖŖøĆ·“Ó¦µÄŃō¼«·“Ó¦ĪŖ£ŗ4OHØDØD4eØD£½O2”ü£«2H2O£¬ŌņŅõ¼«·“Ó¦Ź½ĪŖ£ŗ_______________________________ ”£
ÓŠČĖĢį³ö£¬æÉŅŌÉč¼Ę·“Ó¦2CO£½2C£«O2£Ø”÷H£¾0”¢”÷S£¼0£©Ą“Ļū³żCOµÄĪŪČ¾”£ĒėÄćÅŠ¶ĻŹĒ·ńæÉŠŠ²¢Ėµ³öĄķÓÉ£ŗ__________________________ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŠšŹö“ķĪóµÄŹĒ£ŗ
A£®ÉśĢśÖŠŗ¬ÓŠĢ¼£¬æ¹øÆŹ“ÄÜĮ¦±Č“æĢśČõ
B£®ÓĆĪżŗø½ÓµÄĢśÖŹĘ÷¼ž£¬ŗø½Ó“¦Ņ×ÉśŠā
C£®½šŹōŌŚŗ£Ė®ÖŠ±ČŌŚµĖ®ÖŠøüŅ×ÉśŠā
D£®µē½āČŪČŚµÄĀČ»ÆÄĘÖĘČ”½šŹōÄĘ£¬ÓĆĢś×÷Ńō¼«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŅ¶žĖįĖ×³Ę²ŻĖį£¬ĪŖ¶žŌŖĖį£Ø½į¹¹¼ņŹ½ĪŖHOOC£COOH£¬æɼņŠ“ĪŖH2C2O4£©”£25”ꏱ£¬²ŻĖįµÄµēĄėĘ½ŗā³£ŹżK1£½5.0”Į10£2£¬K2£½5.4”Į10£5£»Ģ¼ĖįµÄµēĄėĘ½ŗā³£ŹżK1£½4.5”Į10£7£¬K2£½4.7”Į10£11”£²ŻĖįøʵÄKsp£½4.0”Į10£8£¬Ģ¼ĖįøʵÄKsp£½2.5”Į10£9”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öĖ®ČÜŅŗÖŠ²ŻĖįµÄµēĄė·½³ĢŹ½£ŗ ”£
£Ø2£©25”ę£¬ĪļÖŹµÄĮæÅØ¶Č¶¼ĪŖ0.1 mol/LµÄNa2C2O4ČÜŅŗµÄpH±ČNa2CO3ČÜŅŗpH______________________£ØĢī”°“ó”±”°Š””±»ņ”°ĻąµČ”±£©”£
£Ø3£©³£ĪĀĻĀ½«0.2 mol/LµÄKOHČÜŅŗ10 mLÓė0.2 mol/LµÄ²ŻĖįČÜŅŗ10 mL»ģŗĻ£¬Čō»ģŗĻČÜŅŗĻŌĖįŠŌ£¬ŌņøĆČÜŅŗÖŠĖłÓŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³Šņ£ŗ____________________”£
£Ø4£©25”ꏱĻņ20 mLĢ¼Ėįøʵı„ŗĶČÜŅŗÖŠÖšµĪ¼ÓČė1.0”Į10£3 mol/LµÄ²ŻĖį¼ŲČÜŅŗ20 mL£¬ÄÜ·ń²śÉś³Įµķ£æ________________£ØĢī”°ÄÜ”±»ņ”°·ń”±£©”£
£Ø5£©³żČ„¹ųĀÆĖ®¹øÖŠµÄCaSO4æÉĻČÓĆĢ¼ĖįÄĘČÜŅŗ“¦Ąķ£¬¶ųŗóÓĆŃĪĖįČܽā£¬Ęä·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ______________________________£»________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖX”¢Y”¢ZĪŖČżÖÖŌ×ÓŠņŹżĻąĮ¬µÄŌŖĖŲ£¬×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌĻą¶ŌĒæČõŹĒ£ŗHXO4£¾H2YO4£¾H3ZO4”£ŌņĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A£®ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗHX£¾H2Y£¾ZH3 B£®·Ē½šŹō»īĘĆŠŌ£ŗZ£¼Y£¼X
C£®µ„ÖŹµÄŃõ»ÆŠŌ£ŗX2£¾Y£¾Z D£®Ō×Ó×īĶāµē×Ó²ćÉĻµÄµē×ÓŹżĻąµČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½ŗĢå·ÖÉ¢ĻµÓėĘäĖü·ÖÉ¢ĻµµÄ±¾ÖŹ²ī±šŹĒ
A£®ŹĒ·ńÓŠ¶”“ļ¶ūĻÖĻó B£®·ÖÉ¢ÖŹĮ£×ÓŹĒ·ń“ųµē
C£®ŹĒ·ńĪČ¶Ø”””””””””” D£®·ÖÉ¢ÖŹÖ±¾¶“óŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«SO2ĶØČėBaCl2ČÜŅŗÖĮ±„ŗĶ£¬Ī“¼ū³ĮµķÉś³É£¬¼ĢŠųĶØČėĮķŅ»ÖÖĘųĢ壬ČŌĪŽ³Įµķ£¬ŌņĶØČėµÄĘųĢåæÉÄÜŹĒ A”¢CO2 B”¢NH3 C”¢NO2 D”¢H2S
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com