
【题目】(1)利用反应![]() 设计成如图甲所示原电池,回答下列问题:
设计成如图甲所示原电池,回答下列问题:
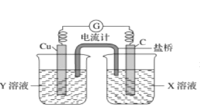
①写出电极反应式:正极________________。
②图中X溶液是_____,Y溶液是______。
③原电池工作时,盐桥中的___________(填“阳”或“阴”)离子向X溶液方向移动。
(2)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图所示,在___(填“阳”或“阴”)极上产生乙烯的电极反应方程式为________。
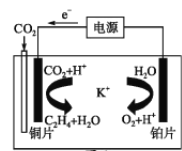
【答案】Fe3+ + e- = Fe2+; FeCl3, CuCl2; 阳, 阴, 2CO2+ 12H+ + 12e- = C2H4 + 4H2O。
【解析】
本题考查电化学知识,原电池中,负极发生氧化反应,正极反生还原反应,溶液或盐桥中的阳离子向正极移动,阴离子向负极移动;电解池中与电源正极相连的是阳极,发生氧化反应,与电源负极相连的是阴极,发生还原反应。
(1)①C为正极,发生还原反应,电极方程式为2Fe3++2e-=2Fe2+,Cu为负极,电极方程式为Cu-2e-=Cu2+;
故答案是:Fe3+ +e- = Fe2+;
②铜被氧化,应为原电池负极,由装置图可知,Y是氯化铜溶液,电解质溶液X是FeCl3;
故答案是:X溶液是FeCl3,Y溶液是CuCl2;
③X是正极池,所以原电池工作时,盐桥中的阳离子向X溶液方向移动;
故答案为:阳;
(2)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯时,在阴极上产生乙烯的电极反应方程式为2CO2+ 12H+ + 12e- = C2H4 + 4H2O;
故答案是:阴;2CO2+ 12H+ + 12e- = C2H4 + 4H2O。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】根据如图所示转化关系,回答下列问题:
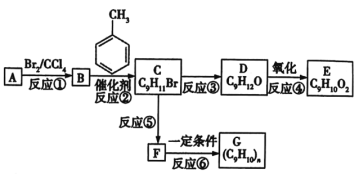
已知:a.![]() ;
;
b. C物质苯环上一卤代物只有两种。
(1)B物质的名称为____________,D物质的结构简式为___________。
(2)反应②的反应类型为_______________,反应⑤的条件为____________。
(3)写出反应⑥的化学方程式:__________________________。
(4)写出D和E反应的化学方程式:_______________________。
(5)反应②还有可能生成一种分子式为C16H18的有机物M,其苯环上的一卤代物也只有两种,写出M的结构简式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释相关问题或实验的离子方程式不正确的是( )
A.NaClO溶液呈碱性:ClO-+H2O![]() HClO+OH-
HClO+OH-
B.向沸水中滴加饱和FeCl3溶液制胶体:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
C.粗盐提纯中除去Mg2+:Mg2++2OH-=Mg(OH)2↓
D.工业上精炼粗铜的阴极反应:Cu-2e-=Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A可用作果实催熟剂。某同学欲以A为主要原料合成乙酸乙酯,其合成路线如下图所示。请回答:
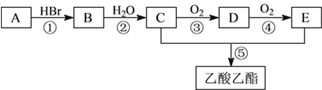
(1)C分子中官能团的电子式是_______________;C的同分异构体F的核磁共振氢谱中,只有一种类型氢原子的吸收峰,F的结构简式是___________。
(2)反应②的化学方程式是__________________________________;反应⑤的化学方程式是__________________________________;
(3)为了检验B中的溴元素,以下操作合理的顺序是_______________(填序号)。
a.加AgNO3溶液 b.加NaOH 溶液 c.加热 d.加稀硝酸至溶液显酸性
(4)实验室制A的化学方程式:__________________________________;在制备中产生SO2会干扰A性质验证,写出SO2与溴水反应的离子方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯生化学名为2,4,4—三氯—2羟基—二苯醚,被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用。则下列有关说法中不正确的是( )
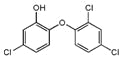
A.物质的分子式为C12H7Cl3O2B.该物质苯环上的一溴取代物有6种
C.该物质中含有四种官能团D.该物质中所有原子都可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据能量关系图,下列分析正确的是

A. 该反应是吸热反应
B. 曲线a的热效应大
C. 该反应的热化学方程式为:4HCl + O2 → 2Cl2 +2H2O + 115.6 kJ
D. 若反应生成2mol液态水,放出的热量高于115.6kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是________,B是________,E是_________。
(2) 写出C元素基态原子的电子排布式_________________________。
(3)写出D元素原子的价电子排布图____________________。
(4) 元素B与D的电负性的大小关系是___________,C与E的第一电离能的大小关系是___________。(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为![]() 。下列说法正确的是
。下列说法正确的是
A. 1L0.1mol·![]() NH4Cl溶液中,
NH4Cl溶液中, ![]() 的数量为0.1
的数量为0.1![]()
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1![]()
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2![]()
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】8.34g FeSO47H2O 样品在隔绝空气条件下受热脱水 过程的热重曲线(样品质量随温度变化的曲线)如图所示。下列说法中正确的是( )
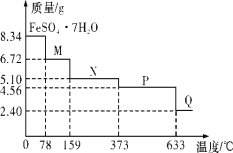
A.温度为 80℃时固体物质 M 的化学式为 FeSO45H2O
B.温度为 200℃时固体物质N 化学式为 FeSO43H2O
C.在隔绝空气条件下由N 到 P 的化学方程式为FeSO4![]() FeO+SO3↑
FeO+SO3↑
D.取 380℃ 时所得的样品 P,隔绝空气加热至 650℃, 得到的固体物质 Q 的化学式为 Fe2O3,同时有两种无色气体生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com