
| A. | C3N4晶体是分子晶体 | |
| B. | C 原子sp3杂化,与4个处于4面体顶点的N 原子形成共价键 | |
| C. | C3N4晶体中C、N原子个数之比为4:3 | |
| D. | C3N4晶体中粒子间通过离子键结合 |
分析 C3N4晶体具有比金刚石更大的硬度,且原子间均以单键结合,则为原子晶体,每个C原子周围有4个N原子,每个N原子周围有3个C原子,形成空间网状结构,C-N键为共价键,比C-C键短,以此解答该题.
解答 解:A.C3N4晶体具有比金刚石更大的硬度,则C3N4晶体是原子晶体,故A错误;
B.因为C的最外层有4个电子,每个电子与另一个N形成C-N(一对共用电子对),因此一个碳原子连接4个N原子,价层电子对数为4,为sp3杂化,因为N的最外层有5个电子,每个电子与另一个C形成N-C(一对共用电子对),因此一个N原子连接3个C原子,成键电子对为3,孤电子对数为1,价层电子数为4,为sp3杂化,故B正确;
C.原子间均以单键结合,则C3N4晶体中每个C原子连接4个N原子,而每个N原子连接3个C原子,所以晶体中C、N原子个数之比为3:4,故C错误;
D.C3N4晶体中构成微粒为原子,微粒间通过共价键合,故D错误.
故选B.
点评 本题考查原子晶体的性质及作用力,为高频考点,明确信息是解答本题的关键,熟悉原子晶体的构成微粒、作用力、空间结构即可解答,题目难度不大,注重知识的迁移能力来分析解答.


科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸的酸性大于碳酸,故硫的非金属性大于碳 | |
| B. | 碳酸的酸性大于次氯酸,故碳的非金属性大于氯 | |
| C. | 硝酸的酸性大于硅酸,故氮的非金属性大于硅 | |
| D. | 氢氟酸的酸性大于氢氯酸,故氟的非金属性大于氯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有离子键和共价键的化合物一定是离子化合物 | |
| B. | 11H2O、12H2O、13H2O互为同位素 | |
| C. | 目前人们已发现的元素种类数目与原子种类数目相同 | |
| D. | 1H的质量数为1,所以氢元素的相对原子质量近似为1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA | |
| B. | 42克由C2H4和C5H10组成的混合气体中含共用电子对数目为9NA个 | |
| C. | 25℃时,50 g 98%浓硫酸和50 g 98%浓磷酸混合后含氧原子数为4NA | |
| D. | 12 g石墨烯(单层石墨)中含有六元环的个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:H2SO4>HClO4 | B. | 原子半径:Na>Mg | ||
| C. | 热稳定性:HCl>HI | D. | 还原性:S2->Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔融态的Al2O3导电、12C转化为14C都属于化学变化 | |
| B. | 根据反应中的能量变化,将化学反应分为“化合、分解、复分解、置换”四类 | |
| C. | 用热的纯碱溶液洗涤沾有油污的器具时涉及化学变化和物理变化 | |
| D. | 将盛有NO2气体的密封烧瓶,放入热水中气体颜色加深的变化是物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
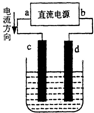
| A. | a为正极 | |
| B. | c极上发生氧化反应 | |
| C. | 电解过程中铜离子移向d极 | |
| D. | 电解过程中,d的电极反应式为:2Cl--2e-=Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H8N2 | B. | CH4N | C. | C3H10N | D. | CH6N3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com