
| A. | 金属Na与乙醇反应比与水反应更剧烈 | |
| B. | 在催化剂存在下,乙醇能被氧气氧化成乙醛 | |
| C. | 乙酸能与碳酸氢钠溶液反应放出CO2 | |
| D. | 在浓硫酸存在下加热,乙酸能与乙醇反应生成乙酸乙酯 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
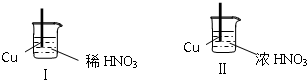
| A. | 两个反应产生的气体不同 | |
| B. | Ⅱ比Ⅰ的反应速率快的原因是因为反应物浓度大 | |
| C. | 浓硝酸在常温下和不同金属反应的现象可能不同 | |
| D. | 浓硝酸与铜反应降价少,所以浓硝酸的氧化性弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(HCO3-)>c(ClO-)>c(OH-) | B. | c(ClO-)>c(HCO3-)>c(H+) | ||
| C. | c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) | D. | c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
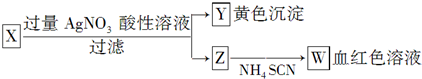
| A. | Z中一定有Fe3+ | B. | X中一定有Fe2+ | C. | Y为AgBr沉淀 | D. | X一定为FeBr2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中有7个主族,7个副族 | |
| B. | VIA族元素原子的最外层电子数均为6 | |
| C. | 碳元素位于第二周期ⅣA族 | |
| D. | 氢分子中的化学键是极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
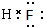 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 Na2CO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) | |
| B. | pH=12的Ba(OH)2溶液和pH=12的NaHCO3溶液中,水电离的c(H+)相等 | |
| C. | 将0.2 mol•L-1 NaA溶液和0.1 mol•L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) | |
| D. | 常温下,pH=4的醋酸与pH=10的NaOH溶液等体积混合后c(OH-)<c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com