
【题目】有机物A 是农药生产中的一种中间体,结构简式如下图所示。下列叙述中正确的是
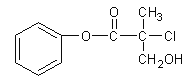
A.1mol A最多能与4mol H2发生加成反应
B.有机物A可以在一定条件下与HBr发生反应
C.有机物A与浓硫酸混合加热,可以发生消去反应
D.1mol A与足量的NaOH溶液反应,最多可以消耗2mol NaOH
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A.  Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.  正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
C.  锌筒作负极,发生氧化反应,锌筒会变薄
锌筒作负极,发生氧化反应,锌筒会变薄
D.  使用一段时间后,电解质溶液的酸性减弱,导电能力下降
使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由多元素组成的化合物Fe-Sm-As-F-O是一种重要的铁系超导材料。下列说法正确的是
A.F的核外电子排布式1s22s22p7
B.Fe3+的轨道表示式![]() 违背了泡利不相容原理
违背了泡利不相容原理
C.N、As同主族,第一电离能N<As
D.电负性F>O>As
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.钠与水反应:Na+2H2O===Na++2OH-+H2↑
B.电解饱和食盐水获取烧碱和氯气:2Cl-+2H2O ![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C.向氢氧化钡溶液中加入稀硫酸:Ba2++OH-+H++SO42-===BaSO4↓+H2O
D.向澄清石灰水中加入少量的NaHCO3溶液:Ca2++2OH-+2HCO3-===CaCO3↓+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.4 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题。
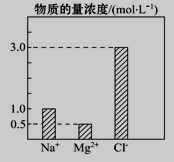
(1)该混合液中,NaCl的物质的量为________mol,含溶质MgCl2的质量为________g。
(2)该混合液中CaCl2的物质的量为_________mol,将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为___________mol·L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物K是某药物的合成中间体,其合成路线如图所示: 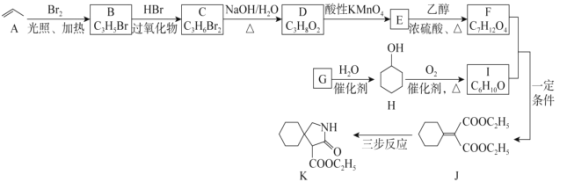
已知:①R1-NH2+R2-COOC2H5![]()
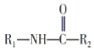 +C2H5OH(R表示烃基或氢原子);
+C2H5OH(R表示烃基或氢原子);
②R-CN ![]() R-CH2NH2(R表示烃基);
R-CH2NH2(R表示烃基);
③HBr与不对称烯烃加成时,在过氧化物作用下,则卤原子连接到含氢较多的双键碳上。
请回答下列问题:
(1)C的化学名称为_____。
(2)D→E的反应类型为_____,F中官能团的名称是_____。
(3)G→H的化学方程式为_____。
(4)J的分子式为________。手性碳原子是指与四个各不相同原子或基团相连的碳原子,则K分子中的手性碳原子数目为_____。
(5) L是F的同分异构体,则满足下列条件的L的结构简式为_________。(任写一种结构即可)
A. 1 mol L与足量的NaHCO3溶液反应能生成2 mol CO2;
B. L的核磁共振氢谱有3组峰且峰面积之比为1:2:3。
(6)请写岀J经三步反应合成K的合成路线:_____(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型冠状病毒肺炎疫情发生以来,科学和医学界积极寻找能够治疗病毒的药物。4-去甲基表鬼臼毒素具有抗肿瘤、抗菌、抗病毒等作用,分子结构如图所示,下列说法错误的是

A.该有机物中有三种含氧官能团
B.该有机物有4个手性碳原子,且遇FeCl3溶液显紫色
C.该有机物分子中所有碳原子不可能共平面
D.1mol该有机物最多可以和2molNaOH、7molH2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物D可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的D为无色黏稠液体,易溶于水,为研究D的组成与结构,进行了如下实验:
(1)称取D 9.0 g,升温使其汽化,测其密度是相同条件下H2的45倍。实验结论:D的相对分子质量为______。
(2)将此9.0 g D在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g。则D的分子式为___________。
(3)另取D 9.0 g,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况)。实验结论:D中含有的官能团的名称是:_________、_________ 。
(4)D的核磁共振氢谱如下图:

实验结论:D的核磁共振氢谱中出现四组峰,即有不同化学环境的氢原子种数为4种,且峰面积之比为________。
(5)综上所述,D的结构简式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用微生物处理含KCN的废水。第一步是微生物在氧气充足的条件下,将 KCN转化成KHCO3和 NH3( 最佳 pH:6.7~7.2);第二步是把氨转化为硝酸:NH3+2O2![]() HNO3+H2O,完成下列填空:
HNO3+H2O,完成下列填空:
(1)写出第一步反应的化学方程式__________________________。
(2)标出第二步反应中电子转移的方向和数目:NH3+2O2![]() HNO3+H2O__________写出产物水的电子式_________。
HNO3+H2O__________写出产物水的电子式_________。
(3)物质KHCO3属于化合物________(选填“离子”或“共价”), 其中属于短周期且原子半径最大的元素是___________(填元素符号):KHCO3 的水溶液pH_____7 (选填“>”、“=”或“<”)。
(4)写出一个能比较 KCN中碳元素和氮元素非金属性强弱的实验事实:__________。
(5)工业上还常用氯氧化法处理含KCN 的废水:
KCN+2KOH+Cl2=KOCN+2KCl+ H2O
2KOCN+4KOH+3Cl2=N2 +6KCl+2CO2+ 2H2O
比较微生物处理法与氯氧化法的优缺点(任写一点)。_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com