
| A.Na > K | B.O2> N2 | C.H2O > H2S | D.SiO2 > CO2 |
科目:高中化学 来源:不详 题型:推断题
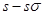 键;D.
键;D.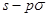 键;E.p—p
键;E.p—p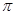 键;F.
键;F.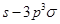 键;G.
键;G.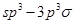 键;H.
键;H.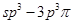 键
键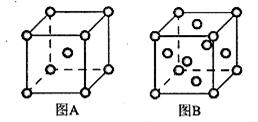
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙醇与浓硫酸170℃共热,制得的气体直接通入溴水,可检验制得的气体是否为乙烯 |
| B.合成氨工业中,利用氨易液化,分离出N2、H2循环使用,可提高氨的产率 |
| C.将(NH4)2Fe(SO4)2·6H2O溶于稀硝酸,滴加KSCN溶液出现血红色,说明试样已变质 |
| D.由ⅠA族和ⅦA族的元素形成的离子晶体,晶体的结构完全相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.晶体中分子间作用力越大,分子越稳定 |
| B.原子晶体中共价键越强,熔点越高 |
| C.冰熔化时水分子中共价键发生断裂 |
| D.氯化钠熔化时离子键未被破坏 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②④⑤ | B.②③④⑤⑨ | C.②③④⑤ | D.②④⑤⑥⑦⑨ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.仅①②③ | B.仅②④⑤ |
| C.仅①③ | D.①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
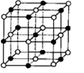
| A.Ti14C13 | B.Ti13C14 | C.Ti6C7 | D.TiC |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com