
| Ͷ�ϱ� | a | b | c | d |
| SO2ƽ��ת����/% | 97.1 | 96.8 | 95.8 | 90.0 |
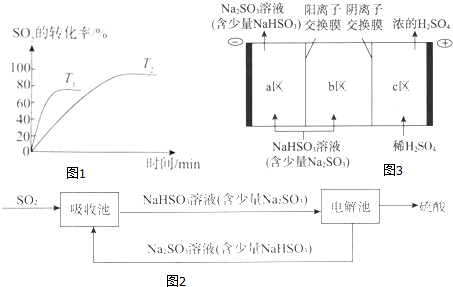
���� ��1�������ݣ����ȹ���ƽ�����¸�ѹ����϶��������ת�����жϣ������¶Ȼ�ѧƽ�������ȷ����ƶ���
��i����Ӧ����ֵģ�����һ�ַ�Ӧ��Ũ�ȿ������������Ӧ��ת���ʣ����ݱ��������жϽ��
ii������Ͷ�ϱ�Ϊ8��10ʱ���������ת���ʣ������ν��
��2�������ճ�������������Һ���������Ӧ�������������ƣ��ݴ���д���ӷ���ʽ��
��i����������������������������������������
ii�����ʱ����Һ�������������������������������õ�����������������Һ��������Ũ�Ƚ��ͣ����¼�������������ӵ�����������������ӣ������ӽ���a��������������ӽ�������������ƣ����������������������ʧȥ���Ӻ�ˮ��Ӧ�������ᣬ�������������������������ӷ�Ӧ���ɶ������ݴ˽��
��� �⣺��1�������ݣ����ȹ���ƽ�����¸�ѹ����֪�¶�Խ�߷�Ӧ����Խ�죬�ﵽ��ѧƽ���ʱ��Խ�̣�����T1��T2����T2��T1���¶����ߣ�
�¶�����ʱƽ�������ȷ����ƶ���SO2��ת���ʼ�С��ƽ���������ƶ�����������Ϊ���ȷ�Ӧ��
�ʴ�Ϊ��������ͬ�����£��¶�Խ�߷�Ӧ����Խ�죬�ﵽ��ѧƽ���ʱ��Խ�̣� �ţ� �¶�����ʱƽ�������ȷ����ƶ���SO2��ת���ʼ�С��
��i����Ӧ����ֵģ�����һ�ַ�Ӧ��Ũ�ȿ������������Ӧ��ת���ʣ�Ͷ�ϱ�[n��SO2����n��O2��]ԽС����������Ũ��Խ��������ת����Խ������b��ת���ʿ�֪��Ͷ�ϱ�[n��SO2����n��O2��]Ϊ��4��15��
�ʴ�Ϊ��4��15��
ii��Ͷ�ϱ�[n��SO2����n��O2��]Ϊ8��10ʱ�����������ת����Ϊ90%������ʼ��������Ϊ4mol���������ʵ���Ϊ5mol��
2SO2��g��+O2��g��?2SO3��g��
��ʼ��mol�� 4 5 0
ת����mol�� 4��90%=3.6 1.8 3.6
ƽ�⣨mol�� 0.4 3.2 3.6
��ƽ��������������������������ΪQ��100%=50%��
�ʴ�Ϊ��50%��
��2�������ճ�������������Һ���������Ӧ�������������ƣ���Ӧ�����ӷ���ʽ��SO2+SO32-+H2O=2HSO3-��
�ʴ�Ϊ��SO2+SO32-+H2O=2HSO3-��
��i�����ݵ��ع���ʾ��ͼ��֪��a���ӵ�Դ�ĸ������ǵ��ص�������c���ӵ�Դ���������ǵ��ص��������ڵ��������������������������������������ʣ�����������a�����������������c������ͼ��ʾ��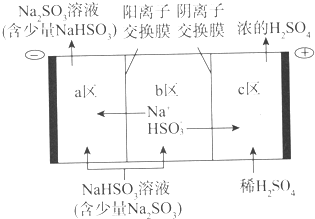 ��
��
�ʴ�Ϊ�� ��
��
ii�����ʱ����Һ�������������������������������õ�����������������Һ��������Ũ�Ƚ��ͣ����¼�������������ӵ�����������������ӣ������ӽ���a��������������ӽ�������������ƣ����������������������ʧȥ���Ӻ�ˮ��Ӧ�������ᣬ�缫��ӦʽΪ��HSO3--2e-+H2O=SO42-+3H+���������������������������ӷ�Ӧ���ɶ�����������c�����˵õ�Ũ�����⣬���õ���������
�ʴ�Ϊ��SO2��
���� ���⿼���˻�ѧƽ���ƶ���Ӱ�����أ���ѧƽ���йؼ��㣬�����е缫��Ӧʽ����д����������жϣ���Ŀ�ۺ��Խ�ǿ����ȷӰ�컯ѧƽ���ƶ�������������ʽ��Ӧ�ã���Ϥ���ع���ԭ���ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

| ʵ����� | 1 | 2 | 3 | 4 |
| ����NaOH��Һ�������mL�� | 20.05 | 20.00 | 18.80 | 19.95 |
| ��ƿ����Һ | �ζ�������Һ | ѡ��ָʾ�� | ѡ�õζ��� | |
| A | �� | �� | ʯ�� | ���ң� |
| B | �� | �� | ���� | ���ף� |
| C | �� | �� | ��̪ | ���ף� |
| D | �� | �� | ��̪ | ���ң� |
| ����Ũ�ȣ�mol•L-1�� | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��С�������ݻ� | |
| B�� | �����������ݻ����䣬ͨ��ϡ������ | |
| C�� | ����������ѹǿ���䣬ͨ��ϡ������ | |
| D�� | ��ʱ�����ɵ�NH3�����ȥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
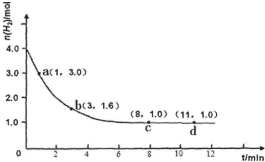 ��ҵ�ϳɰ��ķ�ӦΪ��N2��g��+3H2��g��?2NH3��g����H��0ijʵ�齫3.0mol N2��g����4.0mol H2��g�������ݻ�Ϊ10L���ܱ������У����¶�T1�·�Ӧ�����H2�����ʵ����淴Ӧʱ��ı仯��ͼ��ʾ��
��ҵ�ϳɰ��ķ�ӦΪ��N2��g��+3H2��g��?2NH3��g����H��0ijʵ�齫3.0mol N2��g����4.0mol H2��g�������ݻ�Ϊ10L���ܱ������У����¶�T1�·�Ӧ�����H2�����ʵ����淴Ӧʱ��ı仯��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��ͬѧ��ʵ��Ŀ���Ƿ����Ȼ��ơ��Ȼ��� | |
| B�� | ��ͼ�����ڵIJ��������Ϊ�������� | |
| C�� | ����ʵ�鷽���ɵõ��ϴ�����NaCl���� | |
| D�� | ����ʵ�鷽���ɵõ��ϴ�����CaCl2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʯȼ�ϵ�ֱ�����ã��ٽ��˵�̼���õķ�չ | |
| B�� | �²��ϵ����ƺ�Ӧ�ã���������ǵ�����Ʒ�� | |
| C�� | �ϳ�ҩ����з���ʹ�ã��ٽ���ҽ��������ҵ�ķ�չ | |
| D�� | ���ʵĺ���ʹ�������ũ���������������������ʳΣ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com