
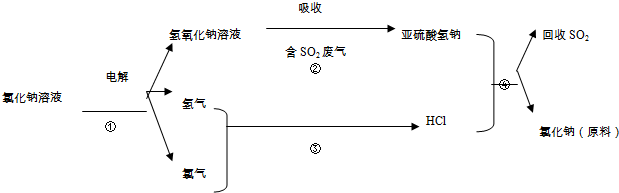
分析 (1)主族元素最高化合价与其族序数相等;
(2)有新物质生成的变化是化学变化,没有新物质生成的变化是物理变化;
(3)根据元素守恒知,食盐中含有Na、Cl元素,根据原子守恒知,其化学式为NaCl;
根据氯原子守恒计算需要氯化钠质量;
(4)二氧化硫是酸性氧化物,能和少量强碱反应生成亚硫酸氢盐和水;亚硫酸氢钠和稀盐酸发生复分解反应生成氯化钠和二氧化硫、水;
(5)吊白块中含有醇羟基、亚硫酸根离子,具有醇和亚硫酸盐性质.
解答 解:(1)主族元素最高化合价与其族序数相等,NaCl中Na元素最高化合价是+1价,所以Na位于第IA族,故答案为:ⅠA;
(2)有新物质生成的变化是化学变化,没有新物质生成的变化是物理变化,根据题干知,蒸馏只是物质状态发生变化,没有新物质生成,所以属于物理变化,故答案为:物理变化;
(3)根据元素守恒知,食盐中含有Na、Cl元素,根据原子守恒知,其化学式为NaCl;
根据氯原子守恒得关系式NaCl----HCl,
设需要氯化钠的质量为x,
NaCl----HCl
58.5 36.5
x 1000t×36.5%
58.5:36.5=x:(1000t×36.5%)
x=$\frac{1000t×36.5%×58.5}{36.5}$=585t,
故答案为:NaCl;585;
(4)二氧化硫是酸性氧化物,能和少量强碱反应生成亚硫酸氢盐和水,反应方程式为NaOH+SO3═NaHSO3;亚硫酸氢钠和稀盐酸发生复分解反应生成氯化钠和二氧化硫、水,反应方程式为NaHSO3+HCl═NaCl+H2O+SO2↑,
故答案为:NaOH+SO3═NaHSO3;NaHSO3+HCl═NaCl+H2O+SO2↑;
(5)吊白块中含有醇羟基、亚硫酸根离子,具有醇和亚硫酸盐性质,能和钠反应生成氢气,能被强氧化剂氧化而发生氧化反应,不含酯基和碳碳不饱和键,所以不能发生皂化反应、聚合反应,故选C、D.
点评 本题考查海水资源综合利用,涉及化学方程式的书写、物质性质判断、物理变化判断等知识点,侧重考查基础知识,熟悉常见元素化合物知识即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
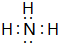 ,空间结构为三角锥形.
,空间结构为三角锥形.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯(苯酚) 加浓溴水,振荡,分液 | |
| B. | 福尔马林(甲酸) 加纯碱溶液,分液 | |
| C. | 乙醇(乙酸) 加NaOH溶液,过滤 | |
| D. | 乙酸乙酯(乙酸) 加饱和Na2CO3溶液,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 在0~a范围内,只发生中和反应 | |
| B. | ab段发生反应的离子方程式为CO32-+2H+═H2O+CO2 | |
| C. | 原混合溶液中NaOH和Na2CO3的物质的量浓度之比为2:1 | |
| D. | c点对应的溶液中还能大量存在Fe2+、NO3-离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧汽油产生的汽车尾气中所含的大气污染物主要是CO,NO、SO2、CO2等 | |
| B. | 乙醇、次氯酸钠溶液均可以将病毒氧化而消毒 | |
| C. | 用纯碱溶液清洗餐具上的油污时,加热可以提高去污能力 | |
| D. | 火力发电是将化学能直接转化为电能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com