
 ���Ϳ����ҩ��
���Ϳ����ҩ��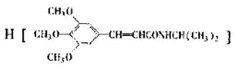 ��·�����£����ַ�Ӧ�������Լ���ȥ��
��·�����£����ַ�Ӧ�������Լ���ȥ��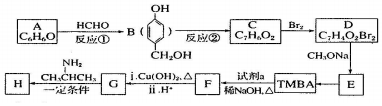
 +H2O��R��R���ʾ��������ԭ�ӣ�
+H2O��R��R���ʾ��������ԭ�ӣ�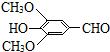 ���Լ�a�ķ���ʽ��C2H4O��
���Լ�a�ķ���ʽ��C2H4O�� +2Br2��
+2Br2��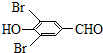 +2HBr��
+2HBr��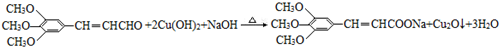 ��
��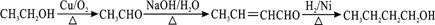 ��
�� ���� A�ķ���ʽΪC6H6O��������HCHO��Ӧ����B����B�Ľṹ��֪AΪ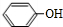 ��B�ķ���ʽΪC7H8O2�����ɵ�C�ķ���ʽΪC7H6O2����Ӧ��Ϊ�ǻ�����Ϊȩ������C�Ľṹ��ʽΪ��
��B�ķ���ʽΪC7H8O2�����ɵ�C�ķ���ʽΪC7H6O2����Ӧ��Ϊ�ǻ�����Ϊȩ������C�Ľṹ��ʽΪ��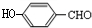 ��C���巢�����ǻ���λȡ������DΪ
��C���巢�����ǻ���λȡ������DΪ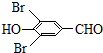 ������ϢI�еķ�Ӧ��֪��D��״��Ʒ�Ӧ����EΪ
������ϢI�еķ�Ӧ��֪��D��״��Ʒ�Ӧ����EΪ ����H�Ľṹ��֪GΪ
����H�Ľṹ��֪GΪ �����ƿ�֪FΪ
�����ƿ�֪FΪ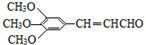 �������ϢII��֪��TMBA��CH2CHO�ڼ�������������F��CH3CH2OHΪԭ���Ʊ�CH3CH2CH2CH2OH���Ƚ��Ҵ�������������ȩ��Ȼ������ȩ������Ϣ���еķ�Ӧ����CH3CH=CHCHO���������ӳ�����CH3CH2CH2CH2OH���ݴ˽��
�������ϢII��֪��TMBA��CH2CHO�ڼ�������������F��CH3CH2OHΪԭ���Ʊ�CH3CH2CH2CH2OH���Ƚ��Ҵ�������������ȩ��Ȼ������ȩ������Ϣ���еķ�Ӧ����CH3CH=CHCHO���������ӳ�����CH3CH2CH2CH2OH���ݴ˽��
��� �⣺A�ķ���ʽΪC6H6O��������HCHO��Ӧ����B����B�Ľṹ��֪AΪ ��B�ķ���ʽΪC7H8O2�����ɵ�C�ķ���ʽΪC7H6O2����Ӧ��Ϊ�ǻ�����Ϊȩ������C�Ľṹ��ʽΪ��
��B�ķ���ʽΪC7H8O2�����ɵ�C�ķ���ʽΪC7H6O2����Ӧ��Ϊ�ǻ�����Ϊȩ������C�Ľṹ��ʽΪ�� ��C���巢�����ǻ���λȡ������DΪ
��C���巢�����ǻ���λȡ������DΪ ������ϢI�еķ�Ӧ��֪��D��״��Ʒ�Ӧ����EΪ
������ϢI�еķ�Ӧ��֪��D��״��Ʒ�Ӧ����EΪ ����H�Ľṹ��֪GΪ
����H�Ľṹ��֪GΪ �����ƿ�֪FΪ
�����ƿ�֪FΪ �������ϢII��֪��TMBA��CH2CHO�ڼ�������������F��
�������ϢII��֪��TMBA��CH2CHO�ڼ�������������F��
��1��������������֪��AΪ ������Ϊ���ӣ�C�Ľṹ��ʽΪ��
������Ϊ���ӣ�C�Ľṹ��ʽΪ�� C�����к��������ŵ������ǣ��ǻ���ȩ����
C�����к��������ŵ������ǣ��ǻ���ȩ����
�ʴ�Ϊ�����ӣ��ǻ���ȩ����
��2����Ӧ�ٵķ�Ӧ��Ϊ���Ӻͼ�ȩ��������ΪB���ԱȽṹ��֪��Ӧ��Ϊ�ӳɷ�Ӧ����Ӧ��Ϊ���ǻ�����Ϊȩ����
�ʴ�Ϊ���ӳɷ�Ӧ��������Ӧ��
��3��������������֪��E�Ľṹ��ʽΪ �Լ�a�ķ���ʽ��C2H4O���ʴ�Ϊ��
�Լ�a�ķ���ʽ��C2H4O���ʴ�Ϊ�� ��C2H4O��
��C2H4O��
��4��C��D�Ļ�ѧ����ʽΪ +2Br2��
+2Br2�� +2HBr���ʴ�Ϊ��
+2HBr���ʴ�Ϊ�� +2Br2��
+2Br2�� +2HBr��
+2HBr��
��5��DΪ �����ڷ������������һ������-OOCH��2��Brԭ������ʱ��-OOCH��2��λ�ã�2��Brԭ�����ʱ��-OOCH��3��λ�ã�2��Brԭ�����ʱ��-OOCH��1��λ�ã��ʹ���2+3+1=6�֣�
�����ڷ������������һ������-OOCH��2��Brԭ������ʱ��-OOCH��2��λ�ã�2��Brԭ�����ʱ��-OOCH��3��λ�ã�2��Brԭ�����ʱ��-OOCH��1��λ�ã��ʹ���2+3+1=6�֣�
�ʴ�Ϊ��6��
��6��FΪ ��������Cu��OH��2����Һ������Ӧ�Ļ�ѧ����ʽ��
��������Cu��OH��2����Һ������Ӧ�Ļ�ѧ����ʽ��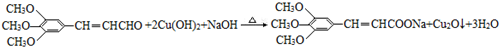 ��
��
�ʴ�Ϊ��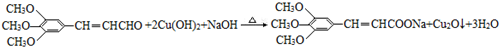 ��
��
��7��CH3CH2OHΪԭ���Ʊ�CH3CH2CH2CH2OH���Ƚ��Ҵ�������������ȩ��Ȼ������ȩ������Ϣ���еķ�Ӧ����CH3CH=CHCHO���������ӳ�����CH3CH2CH2CH2OH�����Ժϳ�����Ϊ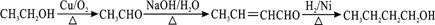 ��
��
�ʴ�Ϊ��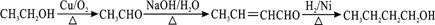 ��
��
���� ���⿼���л��ϳ����ƶϡ�ͬ���칹����жϡ��л���Ӧ���͡���ѧ����ʽ����д���Ƕ��л���ѧ�������ۺϿ��飬ע��������TMBA��H�Ľṹ���л������ʽ�ƶϣ��ϺõĿ���ѧ�����������������Ѷ��еȣ�


 ȫ�ܲ��һ���þ�ϵ�д�
ȫ�ܲ��һ���þ�ϵ�д� ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
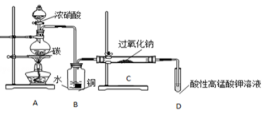 �������ƣ�NaNO2����һ�ֳ�����ʳƷ���Ӽ���ʹ��ʱ�����ϸ������������ij��ȤС���������ʵ��̽������������֪����
�������ƣ�NaNO2����һ�ֳ�����ʳƷ���Ӽ���ʹ��ʱ�����ϸ������������ij��ȤС���������ʵ��̽������������֪����| �ζ����� | 1 | 2 | 3 | 4 |
| KMnO4��Һ���/mL | 20.60 | 20.02 | 20.00 | 19.98 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ��������Ӧ�����ƶ� | |
| B�� | һ�����淴Ӧ�����ƶ� | |
| C�� | ���ƶ� | |
| D�� | ����������Ӧ�����ƶ���Ҳ�������淴Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al�ǵؿ��к������Ľ���Ԫ�أ�������ʹ�ý����Ľ��� | |
| B�� | Al�DZȽϻ��õĽ������ڻ�ѧ��Ӧ������ʧȥ���ӣ����ֻ�ԭ�� | |
| C�� | Al���ڿ��������ȿ����ۻ����ҷ�������ȼ�� | |
| D�� | Al���ڿ��������ȿ����ۻ�����������Ĥ�Ĵ��ڣ��ۻ���Al�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com