
下列对一些实验事实的理论解释正确的是 ( )
选项 | 实验事实 | 理论解释 |
A | 氮原子的第一电离能大于氧原子 | 氮原子2p轨道半充满 |
B | CO2为直线形分子 | CO2分子中C |
C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
 考前必练系列答案
考前必练系列答案科目:高中化学 来源:2015-2016学年河北武邑中学高一下第二次月考化学试卷(解析版) 题型:简答题
I.一定温度下将6mol的A及6molB混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.36mol/(L·min)。求:
xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.36mol/(L·min)。求:
(1)平衡时D的浓度= ,
(2)B的平均反应速率v(B)= ,
(3)x= ,
(4)开始时容器中的压强与平衡时的压强之比为 (化为最箭整数比)
II.将CH4设计成燃料电池,装置如图所示(A、B为多孔碳棒)

(5) (填A或B)处电极入口通甲烷,其电极反应式为 ;
(6)当消耗甲烷的体积为11.2 L(标准状况下)时,则消耗KOH的物质的量为 。
(7)以NH3代替氢气研发燃料电池是当前科研的一个热点。使用的电解质溶液是2mol·L-1的KOH溶液,电池总反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为 ;每消耗3.4gNH3转移的电子数目为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一下第二次月考化学试卷(解析版) 题型:选择题
下列有关实验操作、现象或结论的叙述正确的是________________
A.制备硝基苯的实验中, 水浴加热可以较好的保持恒温条件。
B.乙醇的催化氧化实验中铜丝主要起氧化剂的作用。
C.制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入浓硫酸,最后加入乙酸。
D.在蔗糖溶液中加入少量稀硫酸,水浴加热后,再加入银氨溶液,热水浴加热,没有银镜生成,说明蔗糖没有水解。
E.除去甲烷中混有的少量乙烯,可以将混合气体通过酸性KMnO4溶液
F.用钠可以检验某无水酒精中是否含有水
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一下第二次月考化学试卷(解析版) 题型:选择题
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量 与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:
与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:

下列说法中正确的是( )
A.1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ
B.通常情况下,N2(g)和O2(g)混合能直接生成NO
C.1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下第二次月考化学试卷(解析版) 题型:填空题
某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为________。
(2)Fe2O3是主氧化剂,与Na发生置换反应生成的还原产物为________。
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O。KClO4含有化学键的类型为________,金属晶体K的堆积方式为________。
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为______
__________________________________。
(5)100 g上述产气药剂产生的气体通过碱石灰后得到N2 33.6 L(标准状况)。
①用碱石灰除去的物质为________________;
②该产气药剂中NaN3的质量分数为________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下第二次月考化学试卷(解析版) 题型:选择题
根据原子结构及元素周期律的知识,下列叙述正确的是( )
A.由于分子中氢原子数:H2SO4>HClO4 ,故酸性:H2SO4>HClO4
B.硅处于金属与非金属的过渡位置,硅可用作半导体材料
C.由于氮元素的最低化合价只有-3价,故NH5这种物质不可能存在
D.Cl-、S2-、Ca2+、K+半径逐渐减小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二5月月考化学试卷(解析版) 题型:简答题
(1)在其他条件不变的情况下,起始氢气的物质的量[用n(H2)表示]对N2(g)+3H2(g) 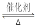 2NH3(g)反应的影响可表示成如图所示的规律(图中
2NH3(g)反应的影响可表示成如图所示的规律(图中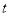 表示温度,
表示温度,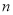 表示物质的量)。
表示物质的量)。
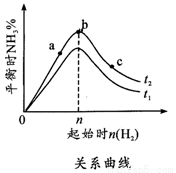
①比较在a、b、c三点处的平衡状态中,反应物N2的转化率最高的是__________。
②若容器容积为1L,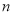 =3mol,反应达到平衡时H2的转化率为60%,则在起始时体系中加入N2的物质的量为__________mol,此条件下(t2)反应的平衡常数
=3mol,反应达到平衡时H2的转化率为60%,则在起始时体系中加入N2的物质的量为__________mol,此条件下(t2)反应的平衡常数 =________。
=________。
③图像中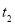 和
和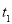 的关系是t2 ______ t1(填“高于”“低于”“等于”或“无法确定”)。
的关系是t2 ______ t1(填“高于”“低于”“等于”或“无法确定”)。
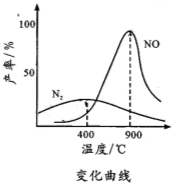
(2)氨气和氧气与145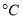 时开始反应,在不同温度和催化剂条件下生成不同产物(如图所示)
时开始反应,在不同温度和催化剂条件下生成不同产物(如图所示)
4NH3+5O2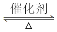 4NO+6H2O
4NO+6H2O
4NH3+3O2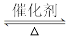 2N2+6H2O
2N2+6H2O
温度较低时以生成________为主,温度高于900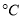 时,NO产率下降的原因是______。
时,NO产率下降的原因是______。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁东北育才学校高一下第二段考化学试卷(解析版) 题型:实验题
某化学实验小组拟用以下装置由乙醇与浓硫酸共热制备乙烯,且进行乙烯的催化氧化实验.
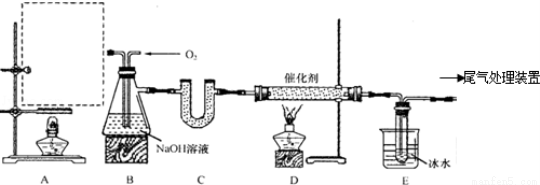
(1)在A处虚线框内绘出该实验装置图.
(2)制取乙烯的化学方程式为 .
(3)装置B中盛有NaOH溶液,除了便于观察乙烯和氧气的流速以外,还具有的作用是:
① ;② .
(4)若E中收集到的物质为CH3CHO,则D中发生反应的化学方程式为 .
(5)用乙醇、浓硫酸共热制乙烯,所得乙烯产率较低,原因可能是 .
A.乙醇部分挥发
B.乙醇部分生成乙醚
C.乙醇被氧化为C、CO、CO2
D.加热速度过快.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁东北育才学校高二下第二段考化学试卷(解析版) 题型:选择题
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列事实不能说明上述观点的是( )
A.苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应
B.乙烯能发生加成反应,乙烷不能发生加成反应
C.甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色
D.苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com