
(1)制备氢氧化铁胶体的化学方程式为 。
(2)碳酸氢钠在水溶液中的电离方程式为 。
(3)能证明Na2SO3溶液中存在SO32-+H2O HSO3-+OH-水解平衡的事实是 (填选项字母)。
HSO3-+OH-水解平衡的事实是 (填选项字母)。
A.滴入酚酞溶液变红,再加入H2SO4溶液后红色退去
B.滴入酚酞溶液变红,再加入氯水后红色退去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去
(4)现有可逆反应:2A(g)+2B(g) C(g)+3D(s),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ. A、B的起始物质的量均为2 mol,Ⅱ.C、D的起始物质的量分别为2 mol和6 mol。以下说法中正确的是 (填选项字母)。
C(g)+3D(s),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ. A、B的起始物质的量均为2 mol,Ⅱ.C、D的起始物质的量分别为2 mol和6 mol。以下说法中正确的是 (填选项字母)。
A.Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的百分组成相同
B.达到平衡时,途径Ⅱ所得混合气密度为途径Ⅰ所得混合气密度的2倍
C.达到平衡时,途径ⅡC的平衡浓度大于途径ⅠC的平衡浓度的2倍
(5)在恒容绝热(不与外界交换能量)条件下进行2A (g)+ B(g) 2C(g)+ D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系: 。
2C(g)+ D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系: 。
| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
科目:高中化学 来源: 题型:
新型净水剂高铁酸钾(K2FeO4 )为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。
)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。
工业上制备K2FeO4的常用方法有两种。
方法Ⅰ:次氯酸盐氧化法。
工艺流程如图所示。
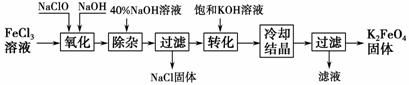
( 1)完成“氧化”过程中反应的化学方程式:
1)完成“氧化”过程中反应的化学方程式: 
 ________FeCl3+________NaOH+________NaClO→________Na2FeO4+________ +________ 。其中氧化剂是________(填化学式)。
________FeCl3+________NaOH+________NaClO→________Na2FeO4+________ +________ 。其中氧化剂是________(填化学式)。
(2)“转化”过程中发生反应的化学方程式为____________________________
______________________________________________________________。
(3)上述工艺得到 的高铁酸钾常含有杂质,可用重结晶法提纯,操作是:将粗产品用________________溶解,然后________________
的高铁酸钾常含有杂质,可用重结晶法提纯,操作是:将粗产品用________________溶解,然后________________
方法Ⅱ:电解法。
以铁为阳极电解氢氧化钠溶液,然后在阳极液中加入KOH。
(4)电解时阳极发生反应生成FeO42-, 该电极反应方程式为________________________________________________________________。
该电极反应方程式为________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
具有单双键交替长链(如:—CH==CH—CH==CH—CH==CH—…)的高分子有可能成为导电塑料。2000年诺贝尔(Nobel)化学奖即授予开辟此领域的3位科学家。下列高分子中可能成为导电塑料的是( )
A.聚乙烯 B.聚丁二烯 C.聚苯乙烯 D.聚乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,下列各组离子能大量共存的是
A.稀硫酸中:K+、Mg2+ 、AlO2-、S2O32-
B.Na2S溶液中:SO42-、K+、Cl-、Cu2+
C.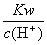 =10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42-
=10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42-
D.通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验“操作和现象”与“结论”对应关系正确的是
| 操作和现象 | 结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 向饱和Na2CO3溶液中通入足量CO2 ,溶液变浑浊 | 析出了NaHCO3 |
| D | 向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液,红色褪去 | 使溶液褪色的气体是乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的分类都正确的是(括号里的是类别)( )。
A.空气( 混合物)、C2H5OH(醇)、H2SO4(离子化合物)、CO2(非电解质) B.液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强电解质)
混合物)、C2H5OH(醇)、H2SO4(离子化合物)、CO2(非电解质) B.液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强电解质)
C.HCl(共价化合物)、CH3COOH(羧酸)、 Na2O2(碱性氧化物)、CH3I(卤代烃)
Na2O2(碱性氧化物)、CH3I(卤代烃)
D.NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯)
查看答案和解析>>
科目:高中化学 来源: 题型:
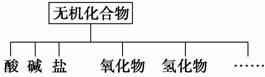
无机化合物可根据其组成和性质进行分类。
(1)如图所示的物质分类方法的名称是______________。
(2)
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ① ②_____ | ③___ ④Ba(OH)2 | ⑤Na2CO3⑥______ | ⑦CO2 ⑧ | ⑨NH3 ⑩H2O2 |
以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥后面。
(3)写出⑦转化为⑤的化学方程式______________________________________
________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在同温同压下,2NH3 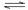 3H2+N2达到平衡时,NH3的转化率为50%,此时平衡混合气的密度与NH3未分解时的密度之比为 ( )
3H2+N2达到平衡时,NH3的转化率为50%,此时平衡混合气的密度与NH3未分解时的密度之比为 ( )
A.1:1 B.2:3 C.3:2 D.2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
(Cl的原子量:35.5)某原子AZX,它的氯化物XCl 5.85g溶于水制成溶液后, 加入2mol/L的AgNO3溶液50mL恰好完全反应.若这种原子原子核内有12个中子,求:
(1)Z值和A值;
(2)X元素在周期表中的位置;
(3)把X的单质放入水中,写出反应的化学方程式.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com