
下列离子方程式表达不正确的是( )
A.碳酸钙和稀盐酸反应:CaCO3+2H+===Ca2++CO2↑+H2O
B.将磁性氧化铁溶于盐酸:Fe3O4+8H+===2Fe2++Fe3++4H2O
C.金属铝加入到NaOH溶液中:2Al+2OH-+2H2O===2AlO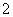 +3H2↑
+3H2↑
D.金属钠与水反应:2Na+2H2O===2Na++2OH-+H2↑
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
温度为T时,向V L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)C(s)+xD(g) ΔH>0,容器中A、B、D的物质的量浓度随时间的变化如图所示。下列说法正确的是( )
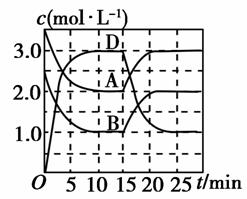
A.反应在前10 min的平均反应速率v(B)=0.1 mol·L-1·min-1
B.该反应的平衡常数表达式K=
C.若平衡时保持温度不变,压缩容器体积平衡向逆反应方向移动
D.反应至15 min时,改变的条件是降低温度
查看答案和解析>>
科目:高中化学 来源: 题型:
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为________;
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
亚硝酸钠(NaNO2)在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛应用,也常用于鱼类、肉类等食品的染色和防腐。但因其有毒,所以在食品行业用量有严格限制。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①NO+NO2+2OH-===2NO +H2O
+H2O
②气体液化的温度:NO2为21 ℃,NO为-152 ℃
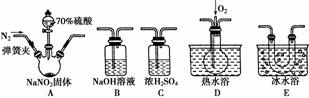
(1)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接)为A、C、________、________、________。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是________________________________________________________________________。
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是_______________________________
________________________________________________________________________。
②装置E的作用是_______________________________________________________。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为________________
________________________________________________________
________________。如果没有装置C,对实验结论造成的影响是__________________
______________________________________________________。
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向x mL 2.0 mol/L的盐酸中投入a g镁铝合金,金属完全溶解,再加入y mL 1.0 mol/L的NaOH溶液,沉淀达到最大值,且质量为(a+1.7)g,则下列说法不正确的是( )
A.x=2y
B.镁铝合金与盐酸反应时转移电子的数目为0.1NA
C.镁铝合金与盐酸反应产生H2的体积在常温常压下大于1.12 L
D.a的取值范围为0.9 g<a<1.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
已知离子反应:Fe3++3SCN-===Fe(SCN)3,具有反应迅速、现象明显等特点,是检验Fe3+常用的方法之一。某化学兴趣小组为探究Fe(SCN)3的性质,做了以下实验:
①取10 mL 1 mol/L FeCl3溶液,滴加3~4滴浓KSCN溶液,振荡后溶液立即变成血红色。
②取少量血红色溶液,滴加少许浓硝酸,静置,溶液变为无色,同时产生大量的红棕色气体混合物A。
③将该气体混合物A通入过量的Ba(OH)2溶液中,产生白色沉淀B和剩余气体C。气体C无色无味,能使燃烧的木条熄灭,可排放到空气中,不会改变空气的成分。
④过滤,向白色沉淀B中滴加少量稀硝酸,沉淀完全溶解,同时产生能使澄清石灰水变浑浊的无色无味气体D。
⑤取②中无色溶液少许,滴加BaCl2溶液,产生不溶于稀硝酸的白色沉淀E。
根据上述实验现象,回答下列问题:
(1)B的化学式为________________;E的化学式为__________。
(2)混合气体A的成分是________________(填化学式)。
(3)兴趣小组同学根据以上实验现象分析得出结论:Fe(SCN)3具有还原性,反应②中被氧化的元素是________________(填元素符号)。
(4)实验②中,还原剂与氧化剂的物质的量之比为_________。
(5)小组同学从上述实验中得到启发,若用SCN-间接检验Fe2+时应注意________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述不正确的是
A.标准状况下,33.6LCO2中含有氧原子数为3NA
B.1 mol OH-和1 mol -OH(羟基)所含质子数均为9NA
C.常温下,100mL 0.1 mol·L-1醋酸钠溶液中含醋酸根的数目小于0.01NA
D.50mL18.4 mol·L-1浓硫酸与足量铜加热反应,生成SO2分子数为0.46NA
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
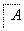
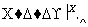
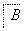
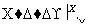
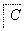
(1)若X是强氧化性气体单质,则A可能是______(填序号)。
a.C b.Al c.Na d.Mg
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,X在A中燃烧产生棕黄色的烟。B的化学式为________;C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示)______ __;检验此C溶液中金属元素的操作方法是
__;检验此C溶液中金属元素的操作方法是 ________
________ ________;向C的溶液中加入氢氧化钠溶液,现象是__________;请
________;向C的溶液中加入氢氧化钠溶液,现象是__________;请 写出此过程中属于氧化还原反应的化学方程式__________________。
写出此过程中属于氧化还原反应的化学方程式__________________。
(3)若A、B、C均为含有同种金属元素的化合物,X是强酸或强碱,则B的化学式为__________,反应①的离子方程式为______________________或________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有一瓶乙二醇和丙三醇的混和物,已知它们的性质如下表,据此,将乙二醇和丙三醇互相分离的最佳方法是
| 物质 | 分子式 | 熔点℃ | 沸点℃ | 密度(g/cm3) | 溶解性 |
| 乙二醇 | C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇 | C3H8O3 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
A.萃取法 B. 结晶法 C.分液法 D.蒸馏法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com