
| A.酒精灯 | B.长直玻璃导管 | C.锥形瓶 | D.冷凝管 |
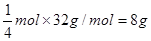 ;
;

科目:高中化学 来源:不详 题型:单选题
| A.往新配制的可溶性淀粉溶液中滴加碘水,溶液显蓝色,用CCl4能从中萃取出碘 |
| B.制备硫酸亚铁铵晶体时,最后在蒸发皿中蒸发浓缩溶液时,只要将溶液蒸干即可 |
| C.用移液管取液后,将移液管稍倾斜放入垂直的容器中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 |
| D.当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.①②③ | C.①③④ | D.②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 N2+3Cu+3H2O中反应物CuO和生成物H2O的质量可以测定铜的近似相对原子质量,实验装置(加热及夹持装置未画出)如下。实验开始时,应先点燃 (填‘‘A”‘‘B”)处酒精灯;c中碱石灰的作用为 。
N2+3Cu+3H2O中反应物CuO和生成物H2O的质量可以测定铜的近似相对原子质量,实验装置(加热及夹持装置未画出)如下。实验开始时,应先点燃 (填‘‘A”‘‘B”)处酒精灯;c中碱石灰的作用为 。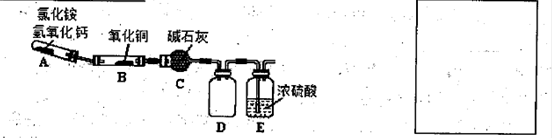
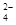 、Cl-等)中提取较纯净的氯化钾晶体及液溴,流程如下:
、Cl-等)中提取较纯净的氯化钾晶体及液溴,流程如下: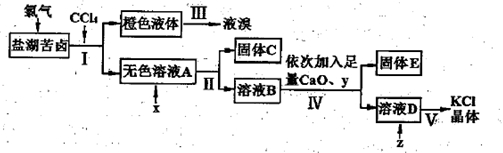
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
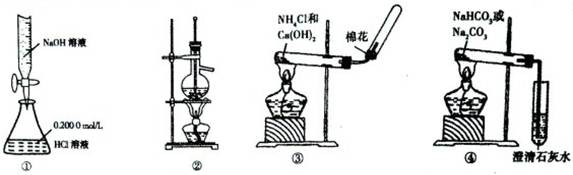
| A.用图①所示装置测定NaOH的浓度 | B.用图②所示装置分馏少量石油 |
| C.用图③所示装置在实验室制备收集氨气 | D.用图④所示装置鉴别碳酸钠和碳酸氢钠 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.滴定管在使用前要用待装液润洗,而容量瓶不用润洗 |
| B.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| C.检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液。 |
| D.将CO2和SO2混合气体分别通入BaC12溶液、Ba(NO3)2溶液中,最终都有沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 目的 | 操作 |
| A | 配制100mL1.0mol/L CuSO4溶液 | 将25gCuSO4·5H2O溶于100mL蒸馏水中 |
| B | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C | 在溶液中将MnO4-完全转化为Mn2+ | 向酸性KMnO4溶液中滴加H2O2溶液至紫色消失 |
| D | 确定NaCl溶液中是否混有Na2CO3 | 取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com