
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.2.3 g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1NA
B.1 mol Na2CO3晶体中含C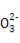 数小于NA
数小于NA
C.惰性电极电解食盐水,若线路中通过NA个电子,则阳极产生气体11.2 L
D.0.1 mol的CaO2中含阴离子数是0.2NA
科目:高中化学 来源:2014高考化学名师选择题专练 电解质溶液练习卷(解析版) 题型:选择题
已知25 ℃时有关弱酸的电离平衡常数如下表:
弱酸 | CH3COOH | HCN | H2CO3 |
电离平衡常数(25 ℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
则下列有关说法正确的是( )
A.a mol/L HCN溶液与b mol/L NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于b
B.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离程度、pH均先增大后减小
C.各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)
D.在0.1 mol/L CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 化学反应中的能量变化练习卷(解析版) 题型:选择题
有关下列四个常用电化学装置的叙述中,正确的是( )
|
|
|
|
图Ⅰ 碱性 锌锰电池 | 图Ⅱ 铅 酸蓄电池 | 图Ⅲ 电解精炼铜 | 图Ⅳ 银锌 纽扣电池 |
A.图Ⅰ所示电池中,MnO2的作用是催化剂
B.图Ⅱ所示电池放电过程中,硫酸浓度不断增大
C.图Ⅲ所示装置工作过程中,电解质溶液中浓度始终不变
D.图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 元素周期表元素周期律练习卷(解析版) 题型:选择题
现有X、Y、Z、W、Q五种短周期元素,原子序数依次增大,Y、Z、W、Q形成的简单离子具有相同的电子层结构,YX3、X2Z、X2Z2、W2Z、W2Z2都是常见的化合物,其中,YX3在常温下呈气态,能使酚酞溶液变红色。下列有关推断正确的是( )
A.简单离子半径:Y>Z>W>Q>X
B.W2Z2与X2Z反应中氧化剂与还原剂物质的量之比为1∶2
C.X能分别与Y、Z、W形成共价化合物
D.Y、W、Q的最高价氧化物对应的水化物两两之间一定相互反应
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 元素周期表元素周期律练习卷(解析版) 题型:选择题
X、Y、Z三种短周期元素,原子半径的大小关系为:r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,其中B和C均为常见的10电子分子。下列说法不正确的是( )
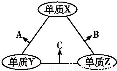
A.X元素位于ⅥA族
B.A不能溶解于B中
C.A和C不可能发生氧化还原反应
D.B的沸点高于C的沸点
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 NA的应用练习卷(解析版) 题型:选择题
设NA代表阿伏加德罗常数的值,下列说法中正确的是( )
A.1 mol NaHSO4晶体含有2NA个离子
B.1 L 2 mol/L明矾溶液经水解可得到氢氧化铝胶体粒子的数目为2NA
C.1 mol C (碳正离子)中含有的电子数为10NA
(碳正离子)中含有的电子数为10NA
D.在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 物质结构与性质练习卷(解析版) 题型:填空题
如图所示为血红蛋白和肌红蛋白的活性部分——血红素的结构式。
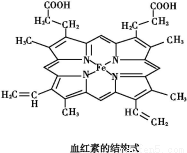
回答下列问题:
(1)血红素中含有C、H、O、N、Fe五种元素,C、N、O三种元素的第一电离能由小到大的顺序是 ,写出基态Fe原子的核外电子排布式: 。
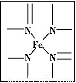
(2)血红素中N原子的杂化方式为 ,在如图的方框内用“→”标出Fe2+的配位键。
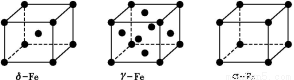
(3)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为 ,δ、α两种晶胞中铁原子的配位数之比为 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 有机合成与推断练习卷(解析版) 题型:填空题
A、B、C、D、E均为有机化合物,转化关系如图所示:
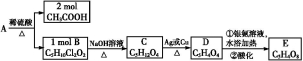
已知:一个碳原子上连有两个羟基时,其结构极不稳定,易发生下列变化,生成较稳定物质:
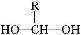
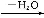
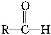
请回答下列问题:
(1)化合物A的分子式: 。
(2)B的结构简式: 。
(3)写出A→B,C→D的有机反应类型:A→B: 反应,C→D: 反应。
(4)B不能发生的反应是 (填序号)。
①氧化反应;②取代反应;③消去反应;④水解反应;⑤加聚反应
(5)写出D与足量的银氨溶液在一定条件下反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题9溶液中的电离平衡练习卷(解析版) 题型:选择题
电导率可用于衡量电解质溶液导电能力大小。室温下,用0.100 mol·L-1 NH3·H2O溶液滴定10.00 mL浓度均为0.100 mol·L-1盐酸和CH3COOH溶液的混合溶液,所得曲线如图所示。下列说法正确的是( )
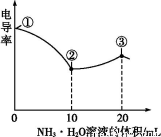
A.①点溶液中c(H+)为0.200 mol·L-1
B.溶液温度高低为①>③>②
C.③点溶液中有c(Cl-)>c(CH3COO-)
D.③点后因离子数目减少使溶液电导率略降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com