
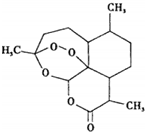
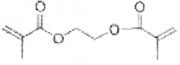
 2015��ŵ��������ѧ��ҽѧ�������й�ҩѧ���������Լ���������ѧ������•���������ձ���ѧ�Ҵ���ǣ����������ڼ����漲�������о�����ȡ�õijɾͣ������������Եط����������أ�������ű�������·�����ͼΪ�����أ����ڸ����ʵ�����˵����ȷ���ǣ�������
2015��ŵ��������ѧ��ҽѧ�������й�ҩѧ���������Լ���������ѧ������•���������ձ���ѧ�Ҵ���ǣ����������ڼ����漲�������о�����ȡ�õijɾͣ������������Եط����������أ�������ű�������·�����ͼΪ�����أ����ڸ����ʵ�����˵����ȷ���ǣ�������| A�� | �����ػ�ѧʽΪC15H20O5 | B�� | �ڹ��������¿��ܷ���ȡ����Ӧ | ||
| C�� | ���������������ӳɷ�Ӧ | D�� | ˮ�����������ű�������õ���Ч |
���� �ɽṹͲʽ��֪�������к�5����״�ṹ����-COOC-��1���������ţ�����������ʼ�C�γ�4����ѧ�������
��� �⣺A���ɽṹ��ʽ��֪�����صķ���ʽΪC15H22O5����A����
B�����м����ڹ��������¿ɷ���ȡ����Ӧ����B��ȷ��
C��������������һ���������������������ӳɷ�Ӧ����C����
D���������в�����ˮ�������Բ�������ˮ��ˮ�����������ű����Ч���ã���D����
��ѡB��
���� ���⿼���л���ṹ�����ʣ�Ϊ��Ƶ���㣬��ȷ�����ż������ʹ�ϵ�ǽⱾ��ؼ������ؿ��������������ʣ���Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
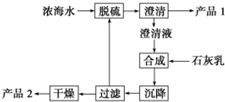 ��ˮ��������ˮ��Դ����ȡ�����ǵ�����ҵ��Ҫ���⣮
��ˮ��������ˮ��Դ����ȡ�����ǵ�����ҵ��Ҫ���⣮| ���� | Na+ | Mg2+ | Cl- | SO42- |
| Ũ��/��g•L-1�� | 63.7 | 28.8 | 144.6 | 46.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | ��; | ���� |
| A | ����� | �ߴ���㷺Ӧ���ڹ��ά��̫���ܵ�غͼ����оƬ | ����а뵼������ |
| B | ������ | �������²��� | Al2O3�۵�ܸ� |
| C | ���ᱵ | ҽѧ���������� | Ba2+�� |
| D | ���� | �������� | ����ˮ��������������ԵĽ������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | W��X��Y��Zԭ�ӵĺ����������������ܺ�Ϊ22 | |
| B�� | ��������Ԫ�ص�ԭ�Ӱ뾶��СΪW��X��Y��Z | |
| C�� | ��W��X��ɵĻ�����ķе��ܵ�����W��Y��ɵĻ�����ķе� | |
| D�� | W��Y���γɼȺ����Թ��ۼ��ֺ��Ǽ��Թ��ۼ��Ļ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
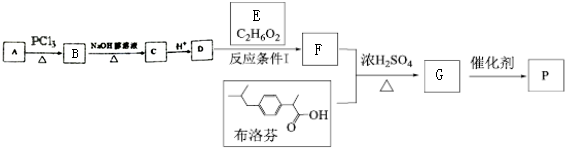
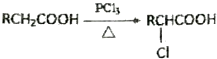
 ��
�� ��
��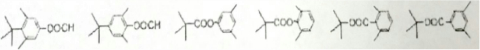 ����2�֣��ٺ��б���������������˴Ź�������Ϊ4��壬�ҷ������Ϊ9��6��2��1��
����2�֣��ٺ��б���������������˴Ź�������Ϊ4��壬�ҷ������Ϊ9��6��2��1���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
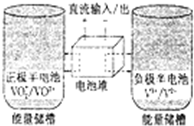 ȫ��������ԭ�����һ�����Ϳɳ��أ���ͬ��̬�ĺ���������Ϊ���������Ļ������ʣ��ֱ��ڸ��Ե����Ե��Һ�����У���ṹԭ����ͼ��ʾ���õ�طŵ�ʱ���Ҳ��еĵ缫��ӦΪ��V2+-e-�TV3+������˵����ȷ���ǣ�������
ȫ��������ԭ�����һ�����Ϳɳ��أ���ͬ��̬�ĺ���������Ϊ���������Ļ������ʣ��ֱ��ڸ��Ե����Ե��Һ�����У���ṹԭ����ͼ��ʾ���õ�طŵ�ʱ���Ҳ��еĵ缫��ӦΪ��V2+-e-�TV3+������˵����ȷ���ǣ�������| A�� | �ŵ�ʱ���Ҳ۷�����ԭ��Ӧ | |
| B�� | �ŵ�ʱ����۵ĵ缫��Ӧʽ��VO2++2H++e-�TVO2++H2O | |
| C�� | ���ʱ��ÿת��1mol���ӣ�n��H+���ı仯��Ϊ1mol | |
| D�� | ���ʱ���������ҺpH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | $\frac{53}{84}$��a��$\frac{53}{62}$ | |
| B�� | a=$\frac{53}{65}$ʱ��m2�й���ΪNa2CO3��NaOH | |
| C�� | a=$\frac{53}{75}$ʱ��m2�й���ΪNa2CO3 | |
| D�� | ��m1=58.4��m2=56.6����m1��NaHCO3Ϊ0.1mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������� | B�� | �������� | C�� | �������� | D�� | ������̼ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com