
H2与ICl的反应分①、②两步进行,其能量曲线如图所示,下列有关说法错误的是

A. 反应①、反应②均为放热反应
B. 反应①、反应②均为氧化还原反应
C. 反应①比反应②的速率慢,与相应正反应的活化能无关
D. 反应①、反应②的焓变之和为ΔH=-218kJ·mol-1
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案科目:高中化学 来源:2017届云南省昆明市新课标高三月考卷(六)理综化学试卷(解析版) 题型:选择题
下列对应化学反应的离子方程式中正确的是
A. 氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B. 向NaAlO2溶液中通入过量的CO2:AlO2-+4CO2+2H2O=Al3++4HCO3-
C. 过量的铁和稀硝酸反应:3Fe + 2NO3- + 8H+ = 3Fe2+ + 2NO↑+ 4H2O
D. 向KAl(SO4)2溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-===2BaSO4↓+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省揭阳市高二下学期第一次月考理科综合化学试卷(解析版) 题型:选择题
直接氨硼烷(NH3·BH3)电池可在常温下工作,装置如下图,该电池的总反应为NH3·BH3+3H2O2=NH4BO2+4H2O。下列说法正确的是( )
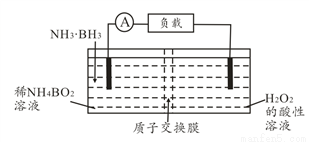
A. 左侧电极发生还原反应
B. 电池工作时,H+通过质子交换膜向负极移动
C. 正极的电极反应式为2H++2e-=H2↑
D. 消耗3.1g氨硼烷,理论上转移0.6mol电子
查看答案和解析>>
科目:高中化学 来源:2017届江西省、临川一中高三1月联考理综化学试卷(解析版) 题型:选择题
化学是一门实用性很强的科学,与社会、环境等密切相关。下列说法错误的是()
A. “静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量
B. 用NH4Cl浓溶液除铁锈,因为NH4 Cl水解显酸性
C. 用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用
D. 在食品袋中放入CaCl2·6H2O,可防止食物受潮
查看答案和解析>>
科目:高中化学 来源:2017届江苏省、溧水高级中学)等六校高三2月联考化学试卷(解析版) 题型:选择题
一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:
CO(g)+Cl2(g) COCl2(g)
COCl2(g)
其中容器Ⅰ中5 min时到达平衡。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法正确的是
A. 容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B. 该反应的正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55 mol
D. 若起始时向容器Ⅰ中加入CO 0.8 mol、Cl2 0.8 mol,达到平衡时CO的转化率大于80%
查看答案和解析>>
科目:高中化学 来源:2017届江苏省、溧水高级中学)等六校高三2月联考化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写不正确的是
A. 用氨水吸收过量的二氧化硫:NH3·H2O+SO2=HSO3-+NH4+
B. 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+ = I2+2H2O
C. 向NH4Al(SO4)2溶液中滴入Ba(OH) 2溶液恰好使SO42-完全沉淀:2Ba2+ + Al3+ + 2SO42- + 4OH- = AlO2- + 2BaSO4↓+ 2H2O
D. 向含0.1mol·L-1 Na2CO3和0.2mol·L-1 NaOH的混合溶液中加入等体积的0.15mol·L-1的硫酸:CO32-+3H++2OH- = 2H2O+HCO3-
查看答案和解析>>
科目:高中化学 来源:2017届浙江省台州市高三上学期期末质量评估考试化学试卷(解析版) 题型:简答题
环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中的氮氧化物(NOx)、CO等有害气体,消除方法有多种。
(1)用稀土等催化剂能将汽车尾气中的CO、NOx、碳氢化合物转化成无毒物质,从而减少汽车尾气污染。已知:
①N2(g)+ O2(g)=2NO(g) △H=180.5 kJ/mol
②2C(s)+ O2(g)=2CO(g) △H=—221kJ/mol
③C(s)+ O2(g)=CO2(g) △H=—393. 5 kJ/mol
写出NO(g)与CO(g)催化转化成N2(g)和CO2(g)的热化学方程式__________________。
(2)①用甲烷催化还原氮的氧化物可消除氮氧化物的污染CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g) ΔH=QkJ·mol-1,写出上述反应的平衡常数表达式_______,已知该反应的平衡常数K随温度升高而减小,则Q_______0(填“>”或“<”或“=”)。
2N2(g)+CO2(g)+2H2O(g) ΔH=QkJ·mol-1,写出上述反应的平衡常数表达式_______,已知该反应的平衡常数K随温度升高而减小,则Q_______0(填“>”或“<”或“=”)。
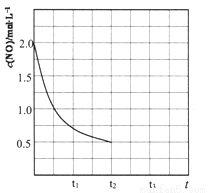
②某温度下,密闭容器中CH4与NO的起始浓度分别为1mol/L、2mol/L,其中c(NO)随时间变化如图所示,t2时达到平衡,保持温度不变在t2时将容器容积压缩到一半,请画出t2-t3 c(CH4)随时间变化的曲线。_______
(3)①为提高反应:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)中的转化率,可以采取在恒压条件下充入稀有气体,解释其原因______________。
N2(g)+CO2(g)+2H2O(g)中的转化率,可以采取在恒压条件下充入稀有气体,解释其原因______________。
②电解吸收法处理氮氧化物废气的基本原理是用硝酸吸收氮氧化物生成NO2-,同时用石墨电极电解将NO2-转化成NO3-,电解条件下循环利用NO3-来处理氮氧化物。写出该法处理NO2总反应的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省台州市高三上学期期末质量评估考试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A. 澄清石灰水中加盐酸:2H++Ca(OH)2=Ca2++2H2O
B. 向NaHCO3溶液中加入NaOH溶液:HCO3-+OH-=CO32-+H2O
C. 氯气溶于水:Cl2+H2O 2H++ClO-+Cl-
2H++ClO-+Cl-
D. 向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三2月联考化学试卷(解析版) 题型:选择题
短周期中的A、B、C、D、E五种元素,原子序数依次增大,A和D,C和E分别同主族,A为短周期元素中原子半径最小的元素,且A与B的原子序数之和等于C的原子序数,C2-与D+的核外电子数相等.则下列说法正确的是( )
A. B与A只能组成BA3化合物 B. E的氧化物对应水化物一定有强的氧化性
C. A、B、C三元素不可能形成离子化合物 D. 第三周期中D原子的原子半径最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com