
����Ŀ��������������Һ�е�ָ��������100 mL 3.9 mol/L Ba(NO3)2��Һ����NO3�����ʵ���Ũ����ͬ����
A.390 mL 0.1 mol/L MgCl2��Һ�е�Cl��
B.200 g Ũ��Ϊ26%���ܶ�Ϊ1.2g/mLNaOH��Һ�е�OH��
C.50 mL 7.8 mol/L Al2(SO4)3��Һ�е�SO42��
D.200 mL 3.9 mol/L CaCl2��Һ�е�Ca2��
���𰸡�B
��������
3.9 mol/L Ba(NO3)2��Һ����NO3�����ʵ���Ũ��Ϊ3.9 mol/L��2=7.8 mol/L��
A. 390 mL 0.1 mol/L MgCl2��Һ�е�c(Cl��)=0.1 mol/L��2=0.2 mol/L���ʲ�ѡA��
B. 200 g Ũ��Ϊ26%���ܶ�Ϊ1.2g/mLNaOH��Һ��c(OH��)= c(NaOH)=![]() 7.8 mol/L����ѡB��
7.8 mol/L����ѡB��
C. 50 mL 7.8 mol/L Al2(SO4)3��Һ��c(SO42��)= 7.8 mol/L��3=23.4 mol/L���ʲ�ѡC��
D. 200 mL 3.9 mol/L CaCl2��Һ�е�c(Ca2��)= 3.9 mol/L��1=3.9 mol/L���ʲ�ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����Ԫ�ص�ԭ�������Ĵ�С˳��ΪC>A>B>D>E��A��Cͬ���ڣ�B��Cͬ���壻A��B�γ����ӻ����A2B���������ӵĵ�������ͬ�����������Ϊ30��D��E���γ�4��10���ӵķ��ӡ��Իش��������⣺
��1��д���������ʵĵ���ʽ��
D�ĵ��ʣ�_________________��
A��B��E�γɵĻ����________________��
D��E�γɵĻ����___________________��
��2��A��B��Ԫ����ɵĻ�����A2B2���ڵĻ�ѧ����_______________��
��3������A������������ˮ������ˮ��Һ�з�Ӧ�����ӷ���ʽΪ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ԭ��Ӧ�ĵ���ת����Ŀ�ͷ���д��������
��1��2K2S + K2SO3 + 3H2SO4= 3K2SO4 + 3S��+ 3H2O _______������_______
��2��2KMnO4 ��5H2O2 + 3H2SO4 = K2SO4��2MnSO4��5O2�� �� 8H2O _______ ������_______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ�����ȡ300mLͬŨ�ȵ����ᣬ���벻ͬ������ͬһþ���Ͻ��ĩ��������ʵ�飬�й������б����£�
ʵ����� | �� | �� | �� |
�Ͻ�����/mg | 510 | 765 | 918 |
(��״��)�������/mL | 560 | 672 | 672 |
��1����������ʵ���Ũ���Ƕ���___��
��2���Ͻ���þ���������������Ƕ���___��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС���ͬѧ��һ�������Ba(OH)2��Һ����μ���ϡ���ᣬ����û��Һ�ĵ���������ʱ��仯������ͼ����С��ͬѧ��ͼ�����������

A.AB����Һ�ĵ����������ϼ�����˵���������ת��Ϊ�ǵ����
B.B���ĵ�������Ϊ0��˵����Һ�м���û�������ƶ�������
C.BC����Һ�ĵ�����������������Ҫ�����ڹ�����Ba(OH)2����������ӵ���
D.aʱ��Ba(OH)2��Һ����ϡ����ǡ����ȫ�к�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���CH3OH������Ҫ���ܼ������ȼ�ϣ���ҵ����CO��H2��һ���������Ʊ�CH3OH�ķ�ӦΪCO(g)+2H2(g)![]() CH3OH(g)�� ��H��
CH3OH(g)�� ��H��
��1�������Ϊ1L�ĺ����ܱ������У�����2molCO��4molH2��һ�������·���������Ӧ�����CO(g)��CH3OH(g)��Ũ����ʱ��ı仯��ͼ����ʾ��
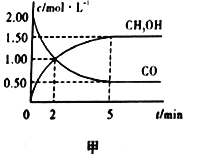
�ٴӷ�Ӧ��ʼ��5min����������ʾ��ƽ����Ӧ����v(H2)=________��
������˵����ȷ����________������ţ���
A. �ﵽƽ��ʱ��H2��ת����Ϊ75%
B. 5min��������ѹǿ���ٸı�
C. �ﵽƽ����ٳ����������Ӧ��������
D. 2minǰv(��)��v(��)��2min��v(��)��v(��)
��2��ij�¶��£���һ��ѹ�����зֱ����1.2molCO��1molH2���ﵽƽ��ʱ�������Ϊ2L���Һ���0.4molCH3OH(g)����÷�Ӧƽ�ⳣ����ֵΪ__________��
��3���״���һ�����͵���������ȼ�ϡ���֪H2(g)��CO(g)��CH3OH(l)��ȼ���ȷֱ�Ϊ285.8kJ/mol��283.0kJ/mol��726.5kJ/mol����״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽΪ________��
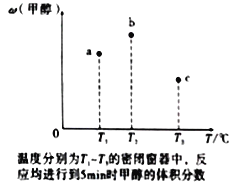
��4�������ݻ���Ϊ1L��a��b��c�����ܱ������������зֱ����1molCO��2molH2�Ļ�����壬�����¶ȣ����з�Ӧ�����������ݵĹ�ϵ��ͼ��ʾ��b�м״������������a�е�ԭ����____________���ﵽƽ��ʱ��a��b��c��CO��ת���ʴ�С��ϵΪ___________��
��5���״���Ϊһ��ȼ�ϻ�������ȼ�ϵ�ء����¶�Ϊ650���������ȼ�ϵ�����ü״���������CO2�Ļ����������Ӧ������缫����Li2CO3��Na2CO3�����������ʡ��õ�صĸ�����ӦʽΪ___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A. 25 ��ʱ����0.1 mol��L��1 NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ�c(Na��)>c(NH)>c(SO![]() )>c(OH��)��c(H��)
)>c(OH��)��c(H��)
B. 25 ��ʱ��NaB��Һ��pH��8��c(Na��)-c(B��)��9.9��10��7 mol��L��1
C. 0.1![]()
![]() ��Һ��
��Һ��![]()
D. ��ͬ���ʵ���Ũ�ȵ�CH3COONa��NaClO�Ļ��Һ�У�������Ũ�ȵĴ�С��ϵ�ǣ�c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������������ε��ԭ����ͼ��ʾ���õ����MnSO4��ҺΪ���Һ��̼��ά��Pt/C�ֱ�Ϊ�缫���ϣ���ص��ܷ�ӦΪMn2��+ 2H2O![]() MnO2 + 2H��+ H2��������˵���������
MnO2 + 2H��+ H2��������˵���������
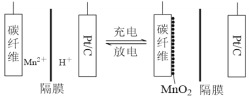
A. ���ʱ��̼��ά�缫������
B. ���ʱ��̼��ά�缫������Һ��pH����
C. �ŵ�ʱ��������Pt/C�缫����������̼��ά�缫
D. �ŵ�ʱ��������ӦʽΪMnO2 + 4H��+ 2e����Mn2��+ 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���淴Ӧm A(g)+n B(g) ![]() p C(g) ��H�����ܱ������н��У���ͼ��ʾ�ڲ�ͬ��Ӧʱ��t ʱ�¶�T��ѹǿP�뷴Ӧ��B�ڻ�������еİٷֺ���B%�Ĺ�ϵ���ߡ������߷����������ж���ȷ����
p C(g) ��H�����ܱ������н��У���ͼ��ʾ�ڲ�ͬ��Ӧʱ��t ʱ�¶�T��ѹǿP�뷴Ӧ��B�ڻ�������еİٷֺ���B%�Ĺ�ϵ���ߡ������߷����������ж���ȷ����

A. T1��T2��P1��P2��m+n��p����H��0
B. T1��T2��P1��P2��m+n��p����H��0
C. T1��T2��P1��P2��m+n��p����H��0
D. T1��T2��P1��P2��m+n��p����H��0
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com