
【题目】在2L密闭容器中,800℃时反应2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= , 已知:K(300℃)>K(350℃),该反应是反应(填“放热”或“吸热”).
(2)图中表示NO2的变化的曲线是 , 用O2的浓度变化表示从0~2s内该反应的平均速率v=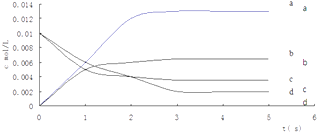
(3)能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂.
【答案】
(1)![]() ;放热
;放热
(2)b;0.0015mol/(L?s)
(3)bc
(4)c
【解析】解(1)可逆反应2NO(g)+O2(g)2NO2(g)的平衡常数k= ![]() ,
,
K(300℃)>K(350℃),说明升高温度平衡向逆反应移动,故正反应是放热反应,
所以答案是: ![]() ,放热;(2)由方程式2NO(g)+O2(g)2NO2(g)可知,平衡时△c(NO):△c(O2):△c(NO2)=2:1:2,由表中数据可知,平衡时c(NO)=
,放热;(2)由方程式2NO(g)+O2(g)2NO2(g)可知,平衡时△c(NO):△c(O2):△c(NO2)=2:1:2,由表中数据可知,平衡时c(NO)= ![]() =0.0035mol/L,曲线b平衡时的浓度为0.0035mol/L,故曲线b表示NO2的浓度变化,
=0.0035mol/L,曲线b平衡时的浓度为0.0035mol/L,故曲线b表示NO2的浓度变化,
由图中数据可知2s内,NO的浓度变化量为0.01mol/L﹣0.004mol/L=0.006mol/L,故v(NO)= ![]() =0.003mol/(Ls),根据速率之比等于化学计量数之比,故v(O2)=
=0.003mol/(Ls),根据速率之比等于化学计量数之比,故v(O2)= ![]() v(NO)=
v(NO)= ![]() ×0.003mol/(Ls)=0.0015mol/(Ls),
×0.003mol/(Ls)=0.0015mol/(Ls),
所以答案是:b,0.0015mol/(Ls);(3)a.始终都存在v(NO2)=2v(O2)关系,故不能说明到达平衡,故a错误;
b.随反应进行气体的物质的量减小,压强增减小,容器内压强保持不变,说明到达平衡,故b正确;
c.不同物质表示的正逆速率之比等于化学计量数之比,反应到达平衡,故v逆(NO)=2v正(O2),说明到达平衡,故c正确;
d.反应混合气体的质量不变,容器的体积不变,密度始终不变,故容器内物质的密度保持不变,不能说明到达平衡,故d错误;
故选bc;(4)a.及时分离出NO2气体,平衡向正反应移动,但反应速率降低,故a错误;
b.适当升高温度,反应速率增大,平衡向逆反应移动,故b错误;
c.增大O2的浓度,反应速率增大,平衡向正反应移动,故c正确;
d.选择高效的催化剂,增大反应速率,不影响平衡移动,故d错误;
故选c.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效),以及对化学平衡状态的判断的理解,了解状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等.


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
【题目】某学习小组做电浮选凝聚法净化污水的实验时,同学们发表了如下看法,其中错误的是( )
A.两个电极都可选用Fe片
B.电源电极接反时仍能产生一定净水效果
C.反应中产生的H2会将Fe3+还原成Fe2+
D.电浮选凝聚法用于工业污水处理时要注意通风,防止爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作助剂,在化学工业和制药工业中也用作氧化剂,应用领域十分广泛。
实验室中红矾钠可用铬铁矿(主要成分:FeO·Cr2O3)利用以下过程来制取。
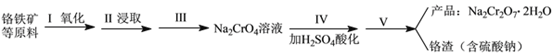
(1)步骤I中反应的化学方程式为:4FeO·Cr2O3(s)+8Na2CO3(s)+7O2 (g)![]() 8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) △H<0该反应的化学平衡常数的表达式为__________________________。
8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) △H<0该反应的化学平衡常数的表达式为__________________________。
(2)在常温下该反应速度极慢,下列措施中能使反应速率增大的是_____________________________ 。
a.升高温度 b.及时转移生成CO2 c.将原料粉碎 d.增加纯碱的用量
(3)步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是__________________________、____________________________。
(4)步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是_____________________________________。
(5)步骤Ⅳ酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知外电路中,电子由b极流向锌.有关如图所示的装置分析不合理的是( ) 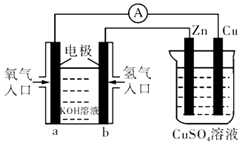
A.该装置中Cu极为正极
B.当铜极的质量变化为32 g时,a极上消耗的O2在标准状况下的体积为5.6 L
C.b极反应的电极反应式为H2﹣2e﹣+2OH﹣═2H2O
D.一段时间后锌片一极质量增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中充入A(g)和B(g),它们的初始浓度均为2molL﹣1 , 在一定条件下发生反应:A(g)+B(g)2C(g).该温度下,此反应的平衡常数为4,则A的转化率为( )
A.30%
B.40%
C.50%
D.60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.向盐酸中滴加氨水:H++OH﹣═H2O
B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O
C.向Na2S2O3溶液中通入足量氯气:S2O ![]() +2Cl2+3H2O═2SO
+2Cl2+3H2O═2SO ![]() +4Cl﹣+6H+
+4Cl﹣+6H+
D.铜溶于稀硝酸:3Cu+8H++2NO ![]() ═3Cu2++2 NO↑+4H2O
═3Cu2++2 NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展,像电一样,氢是一种需要依靠其他能源如石油、煤、原子能等的能量来制取的所谓“二级能源”,而存在于自然界的可以提供现成形式能量的能源称为一级能源,如煤、石油、太阳能和原子能等.
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是
A.电解水
B.锌和稀硫酸反应
C.光解海水
D.以石油、天然气为原料
(2)氢气燃烧时耗氧量小,发热量大.已知,热化学方程式为:
C(s)+O2(g)=CO2(g);△H=﹣393.5kJmo﹣1L
2H2(g)+O2(g)=2H2O(l);△H=﹣571.6kJmo﹣1L
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是 .
(3)氢能源有可能实现能源的贮存,也有可能实现经济、高效的输送.研究表明过渡金属型氢化物(又称间充氢化物),在这类氢化物中,氢原子填充在金属的晶格间隙之间,其组成不固定,通常是非化学计量的,如:LaH2 . 76、TiH1.73、CeH2.69、ZrH1.98、PrH2.85、TaH0.78 . 已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为10.64g/cm3,相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请分析细胞内4种重要有机物的组成及功能,回答下列问题:
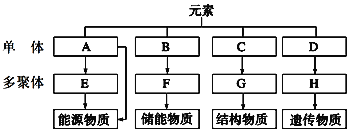
(1)A一般是指________;E在动物细胞中是指____________,在植物细胞中主要是________。
(2)F是指__________,除此之外,脂质还包括__________和固醇。
(3)C是指__________,由m个C构成G物质时,其相对分子质量最多可减少____________。
(4)D是指____________,生物体内的H分为________和________两大类。(写中文名称)
(5)四大有机物都含有的化学元素是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com