
���� ��1�����ݸ�˹�������ж�����;������֮��Ĺ�ϵ��
��2���÷�Ӧ�������ȷ�Ӧ����Ӧ����е�������С�����������������
��3��;��I����C3H8��g��+5O2��g���T3CO2��g��+4H2O��l����H=-a kJ•mol-1
;��II����C3H8��g���TC3H6��g��+H2��g����H=+b kJ•mol-1
��2C3H6��g��+9O2��g���T6CO2��g��+6H2O��l����H=-c kJ•mol-1
��2H2��g��+O2 ��g���T2H2O��l����H=-d kJ•mol-1 ��Ӧ��=��Ӧ��+��Ӧ�ۡ�$\frac{1}{2}$+��Ӧ�ܡ�$\frac{1}{2}$���ݸ�˹�������жϸ�����Ӧ֮��Ĺ�ϵ��
��� �⣺��1�����ݸ�˹���ɣ�ú��Ϊȼ�ϲ�����һ����ɻ��Ƿ�������ɣ���Ӧ��Ͳ������ֵ��һ���ģ�������;�����ʱ�ֵһ�����ų�������һ����
�ʴ�Ϊ�����ڣ�
��2������C3H8��g���TC3H6��g��+H2��g�� �ķ�Ӧ�С�H��0���÷�Ӧ�����ȷ�Ӧ����Ӧ����е�������С�����������������
�ʴ�Ϊ��С�ڣ�
��3��;��I����C3H8��g��+5O2��g���T3CO2��g��+4H2O��l����H=-a kJ•mol-1
;��II����C3H8��g���TC3H6��g��+H2��g����H=+b kJ•mol-1
��2C3H6��g��+9O2��g���T6CO2��g��+6H2O��l����H=-c kJ•mol-1
��2H2��g��+O2 ��g���T2H2O��l����H=-d kJ•mol-1 ��Ӧ��=��Ӧ��+��Ӧ�ۡ�$\frac{1}{2}$+��Ӧ�ܡ�$\frac{1}{2}$���ݸ�˹�������жϸ�����Ӧ֮��Ĺ�ϵ����-a=b+$\frac{1}{2}$��-c-d��������b=-a+$\frac{1}{2}$��c+d����2b=c+d-2a����b=$\frac{c}{2}$+$\frac{d}{2}$-a���ʴ�Ϊ��b=$\frac{c}{2}$+$\frac{d}{2}$-a��
���� ���⿼��ѧ����˹���ɵ�Ӧ���Լ���Ӧ�������뷴Ӧ�����������֮��Ĺ�ϵ�����Ը�����ѧ֪ʶ���лش��ѶȲ���


 Сѧ��ѧ������ѿڶ���ϵ�д�
Сѧ��ѧ������ѿڶ���ϵ�д� ������Ӧ�������������ϵ�д�
������Ӧ�������������ϵ�д� �㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
�㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
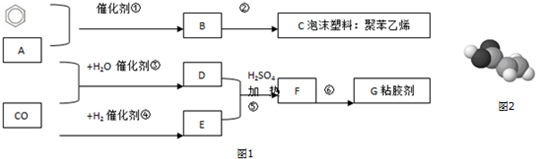

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����к� | B�� | ����ȼ�� | ||
| C�� | Ũ�����ϡ�� | D�� | Ba��OH��2•8H2O��NH4Cl�����壩��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SiO3 | B�� | H3PO4 | C�� | H2SO4 | D�� | HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
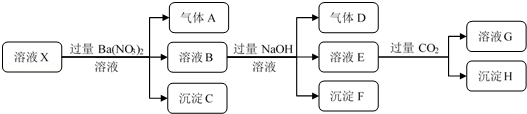
| A�� | ������������ʵ�鲻��ȷ����ҺX���Ƿ���Fe3+ | |
| B�� | ����HΪAl��OH��3 | |
| C�� | ��Һ��һ������H+��Al3+��NH4+��Fe2+��SO42-��Cl- | |
| D�� | ����ҺXΪ100 mL������������AΪ112 mL�����������X��c��Fe2+��=0.15 mol•L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���������� | ���� |
| A | ȡ������Һ���Թ��У��μ�BaCl2��Һ���а�ɫ�������ɣ���ϡ����������ܽ� | ��Һ�к���Ag+��SO42- |
| B | ȡ������Һ���Թ��У��μ�������ˮ����Һ����ɫ��Ϊ��ɫ | ��Һ�к���Br- |
| C | ȡ������Һ���Թ��У��μ�Ũ����������Һ���ȣ��Թܿ�ʪ��ĺ�ɫʯ����ֽ���� | ��Һ�к���NH4+ |
| D | ȡ������Һ���Թ��У��μ�������ˮ���ٵμ�KSCN��Һ����Һ���ɫ | ԭ��Һ�к���Fe2+ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 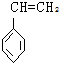 | B�� | 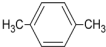 | C�� | 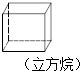 | D�� | 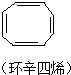 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
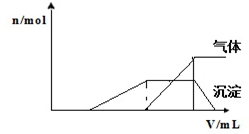 1Lij�����Һ�����ܺ��е����������
1Lij�����Һ�����ܺ��е����������| ���ܴ������е������� | H+ NH4+ Al3+ K+ |
| ���ܴ������е������� | Cl- Br- I?ClO? AlO2- |
| Cl2���������״���� | 2.8L | 5.6L | 11.2L |
| n��X-�� | 1.25mol | 1.5mol | 2mol |
| n��Y-�� | 1.5mol | 1.4mol | 0.9mol |
| n��Z-�� | amol | 0 | 0 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com